冠状动脉造影作为冠脉介入诊断的“金标准”,在心血管疾病诊疗中发挥着重要作用。然而,它仅能提供血管轮廓的二维图像,难以揭示血管内部的复杂情况。随着医学技术的不断进步,血管腔内影像学及功能检测技术应运而生,带给我们更真, 更细, 更全的信息, 极大地提升了冠脉介入诊断的精确性和可靠性。本文将聚焦于IVUS(血管内超声)技术,FFR(冠状动脉血流储备分数),OCT(光学相干断层扫描),从其基本原理、测量方法及常见病变影像解析三个方面展开,帮助读者快速了解这些技术如何助力冠脉介入诊断的精准化。
IVUS的基本原理
IVUS(超声)以特定波长的高频声波及其反射波,测量冠脉组织在此频率下的声阻抗,并将结果以可视化的方法显示。
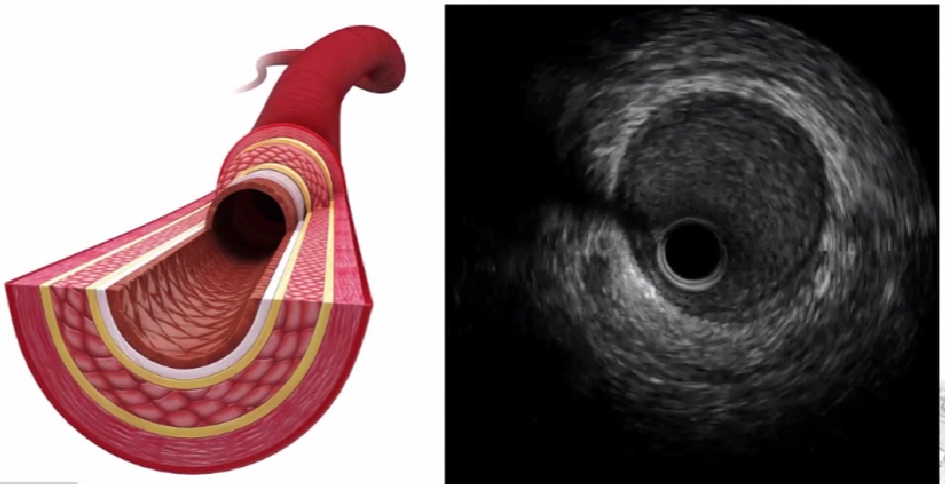
在临床上,超声导管探头类型有两种:
①机械旋转式探头:
探测晶体为单片,在驱动轴上旋转,1800转/每分钟40 MHz,单片晶体,实时成像

40 MHz
②相控阵式探头:
探测晶体不需要旋转(VolcanoTM)
20 MHz,64 片晶体,合成图像

20 MHz
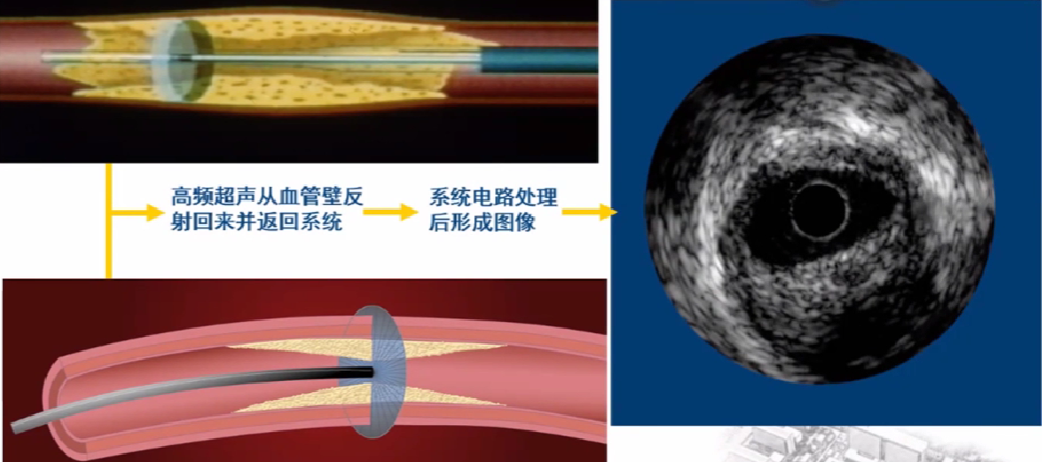
IVUS成像原理
1、正常血管在超声下的影像
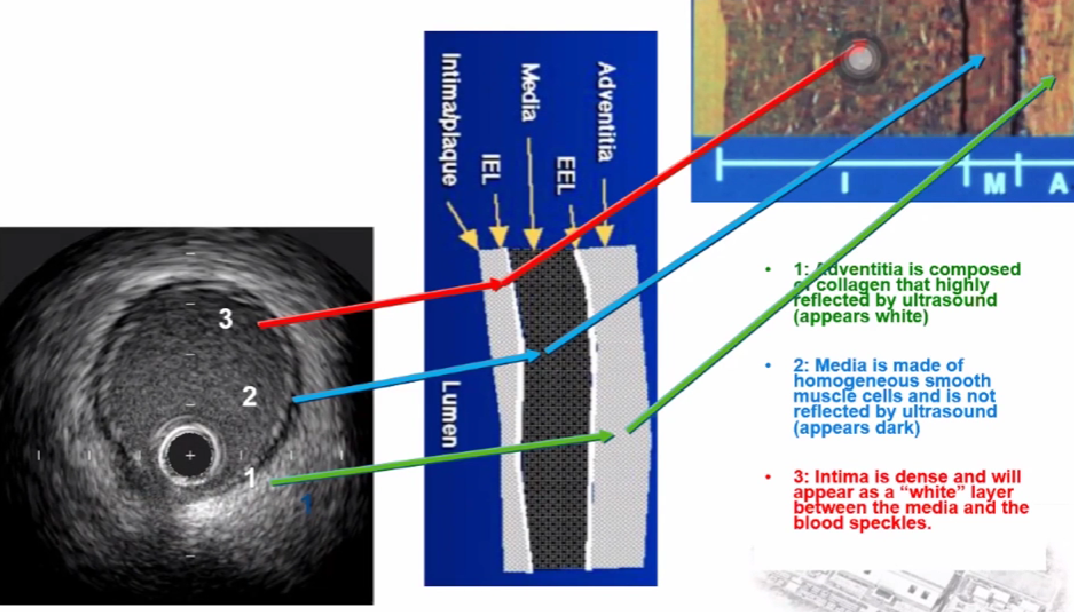
2、不同组织在超声下的影像
低回声的一般是脂质斑块;
等回声的一般是纤维斑块;
高回声是钙化的斑块。
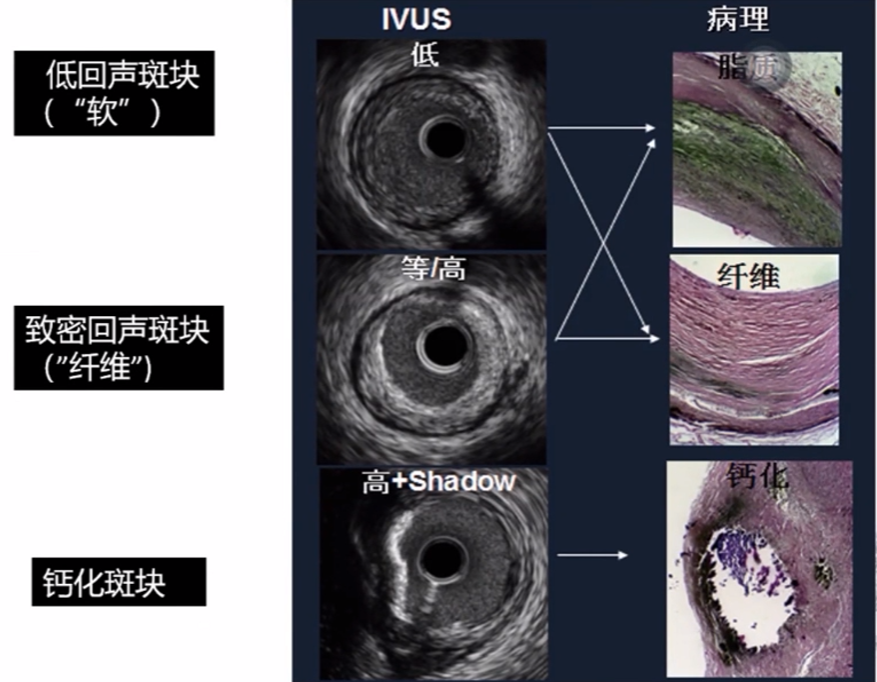
3、动脉血管IVUS基本图像
正常动脉IVUS截面上有什么呢?
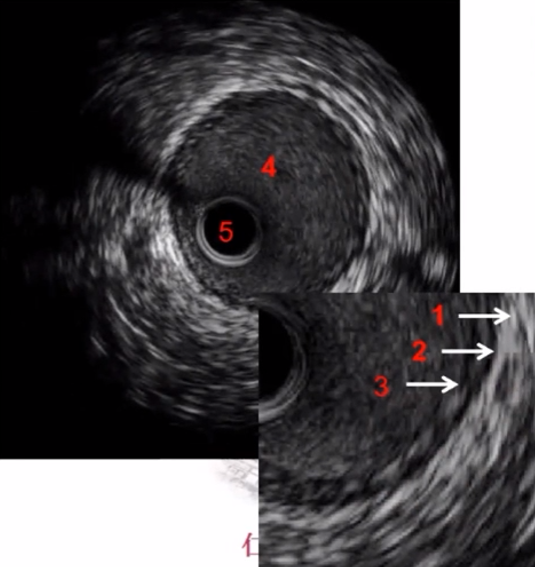
1、血管外膜层: 回波密集,纤维蛋白和胶原蛋白;
2、血管中膜层: 无回波层,平滑肌细胞;
3、血管内膜层: 回波相对密集;
4、管腔: 血液;
5、盲区: 导管;
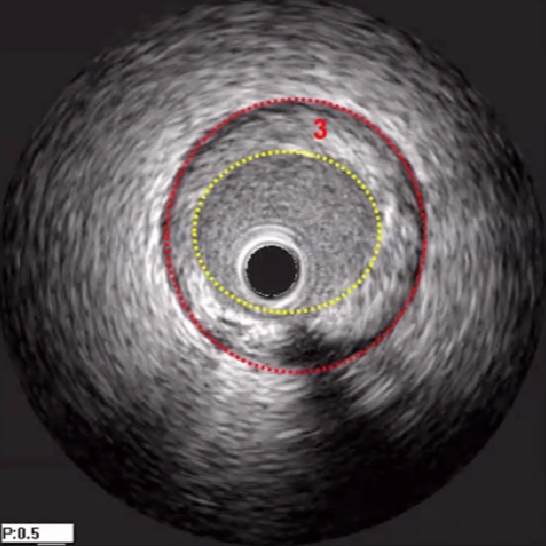
两个边界:①中膜层,连续的无回声;②血流,低回声,闪烁 流动区域;中间(3)即为斑块.
4、心血管内超声影像
血管毗邻结构1,通常用作判断位置匹配的标记
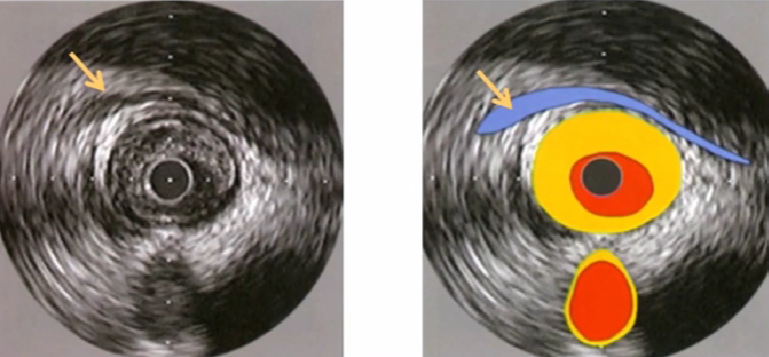
心包腔 分析与血管关系 与心肌桥鉴别
血管毗邻结构2,通常用作判断位置匹配的标记
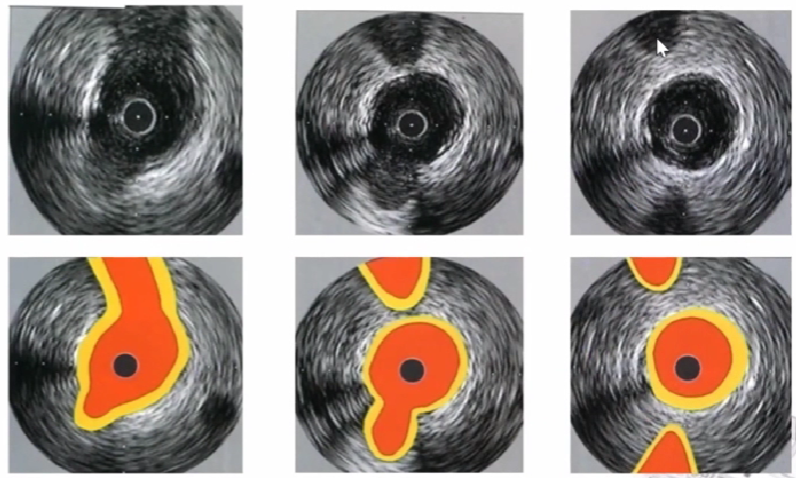
动脉侧支 汇入成像血管腔
血管毗邻结构3,通常用作判断位置匹配的标记
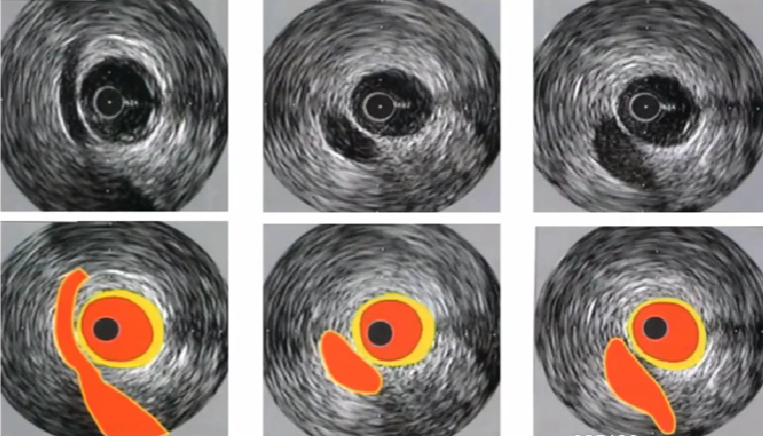
静脉与动脉平行或交叉,不与成像管腔相连,收缩期压缩。
基本测量方法及概念
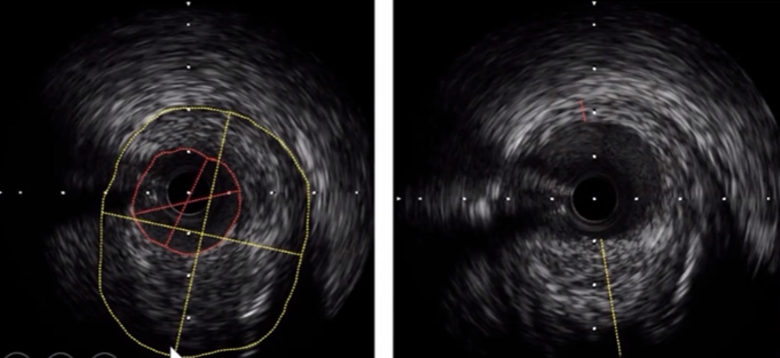
基本测量: 外弹力膜(EEM)
EEM横截面积(lumen CSA): EEM边界围绕的面积;
EEM最小管腔直径: 通过EEM中心点的最小直径;
EEM最大管腔直径: 通过EEM中心点的最大直径;
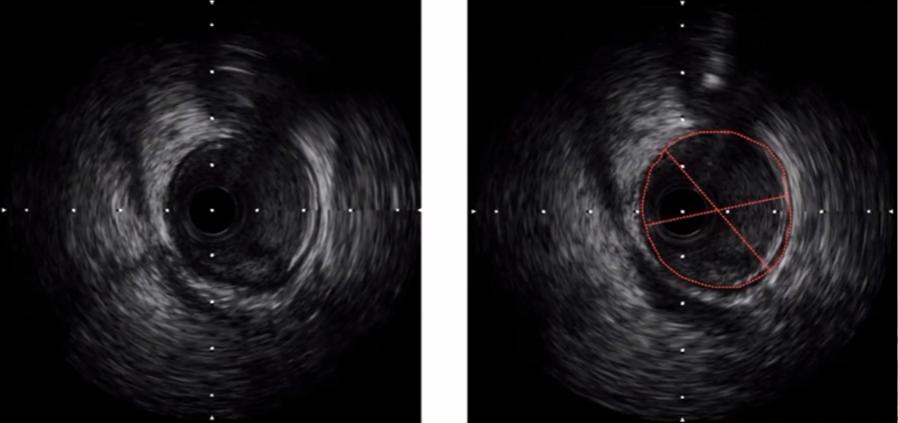
基本测量: 管腔
管腔横截面积(lumen CSA): 管腔边界前缘围绕的面积;
最小管腔直径: 通过管腔中心点的最小直径;
最大管腔直径: 通过管腔中心点的最大直径;
基本测量: 斑块(P&M)
斑块横截面积(lumen CSA): EEM面积一管腔面积;
斑块负荷: 斑块横截面积/EEM横截面积(不是管腔狭窄率);
最小斑块厚度: 内膜前沿至EEM最小距离;
最大斑块厚度: 内膜前沿至EEM最大距离;
斑块偏心指数: (最大斑块厚度一最小斑块厚度)/最大斑块厚度;
血管内超声的临床应用
IVUS冠脉介入适应症: 诊断、指导、评估临界病变、模糊病变、复杂、特殊病变、左主干病变, 开口及分叉病变, CTO病变, 桥血管病变, 支架植入术评估, 晚期支架并发症。
血管内超声检查注意事项:
-
现有超声导管均为一次性使用标准,为了图像质量、安全和避免交叉感染不要重复使用。
-
超声导管不能打折,操作轻柔,勿送入远端细小血管以免造成损伤。
-
推送导管不能越过指引导丝,靶血管显著狭窄先行球囊预扩,不能强行通过。
-
超声导管必需推送至病变的远端,回撤至主干开口,获取完整靶血管信息,防止遗漏病变。
-
血管狭窄、迂曲并钙化显著时,先手动回撤感觉阻力,阻力大不宜采用自动回撤装置。
血管内超声检查并发症: 并发症概率低于其他介入器材,操作不当术前准备不充分可以造成并发症:
-
血管痉挛;
-
血管腔严重狭窄时,造成心肌缺血;
-
血管损伤(夹层、血肿);
-
血栓并栓塞;
-
偶见室颤;
-
钩脱支架、导管卡住或断裂;
-
支架纵向缩短,尤其是机械旋转式导管。
1、超声支架术评估
支架截面积和直径测量
支架截面积:支架边界包绕区域。
最大、最小支架直径:经过支架中心的最大、最小直径。
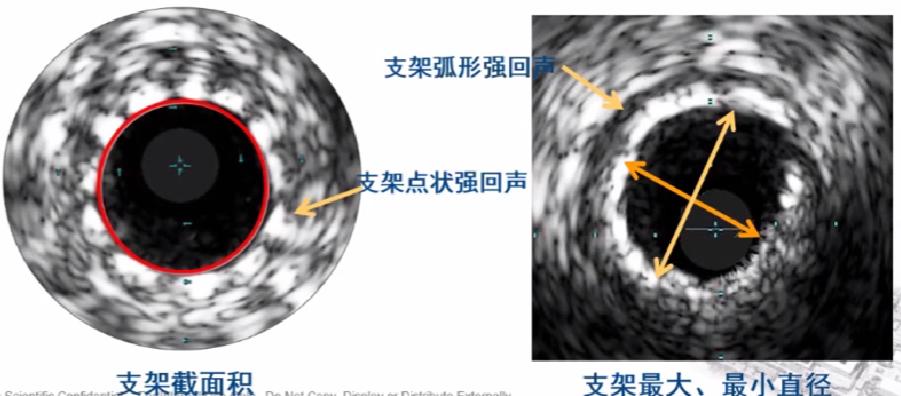
理想支架术的IVUS影像
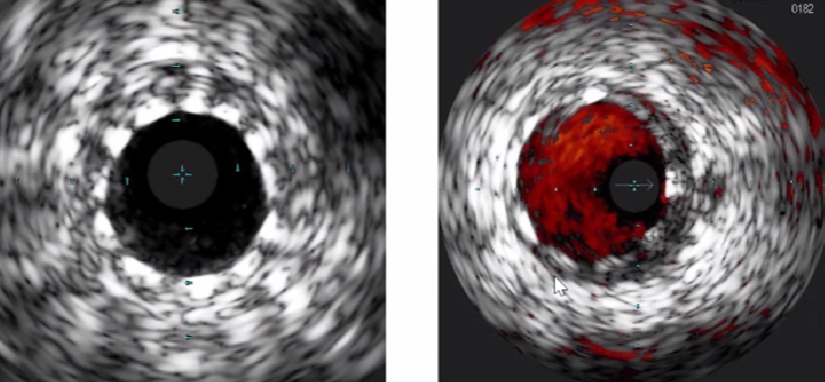
支架贴壁不良
≥1个以上支架柱与管壁之间存在间隙,支架后方有血流回声。
灰阶超声
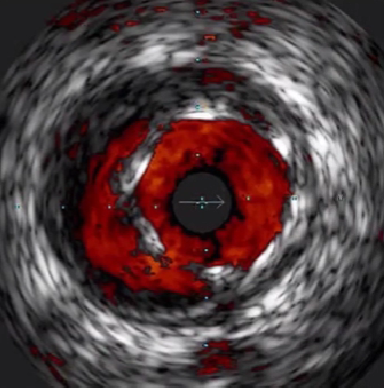
彩色血流
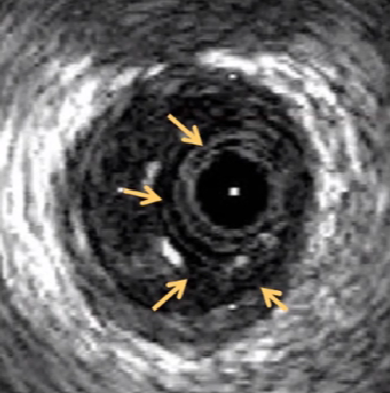
支架膨胀不全
受斑块钙化、分布形态和负荷影响,支架膨胀形态非正圆、不对称。
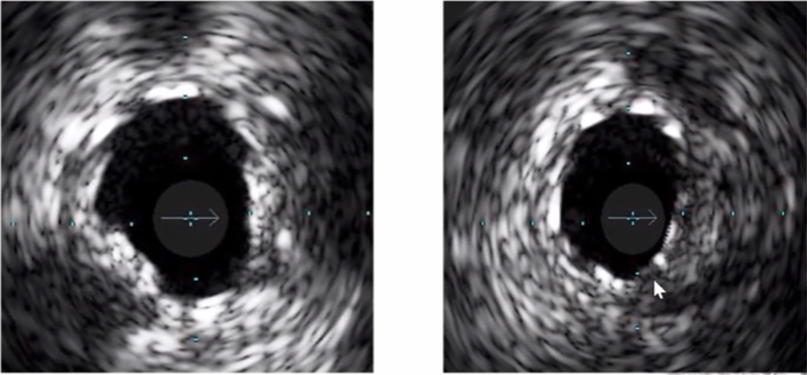
2、横截面斑块影像
根据截面上斑块形态分类
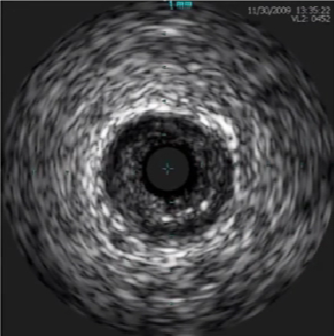
向心性斑块
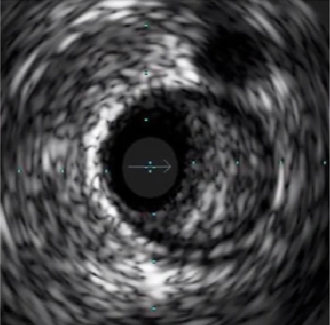
偏心性斑块
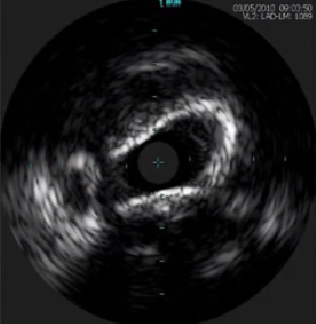
不规则斑块
根据回声强度对斑块分类
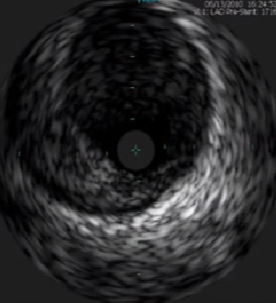
低回声斑块:脂质成分为主
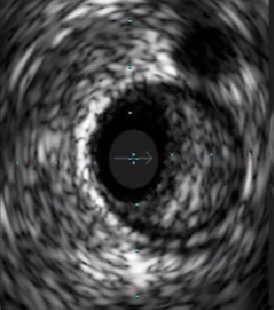
等回声斑块:纤维脂质成分
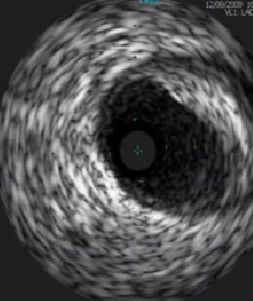
强回声斑块:
致密纤维成分或钙化
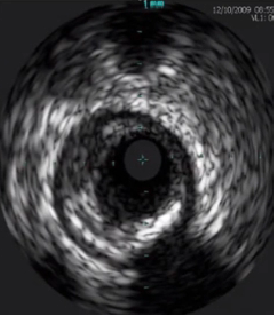
混合性斑块:
各种斑块组织成分
3、长轴界面斑块分布特性
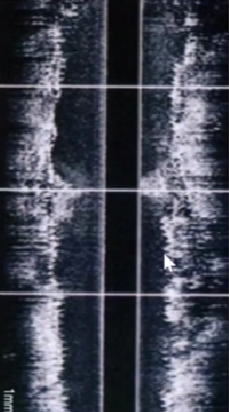
局限性病变
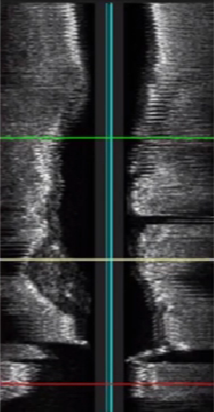
节段性病变
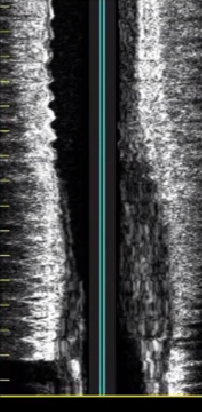
弥漫性病变
4、钙化斑块影像
声影前缘出现在斑块厚度管腔侧50%以内为表浅钙化。
声影前缘出现在斑块厚度外弹力膜侧50%以内为深层钙化。
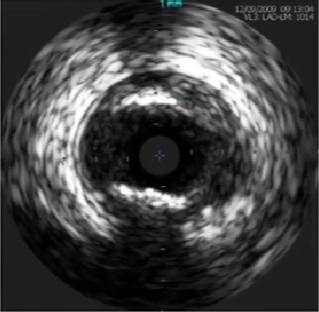
表浅钙化
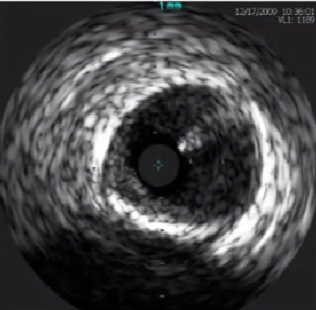
深层钙化
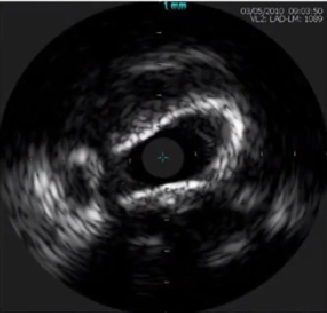
全层钙化
根据钙化斑块沿管腔分布弧度分级:
I级: ≤90°
I级: 91° —180°
Ⅲ级:181° —270°
Ⅳ级: >271°
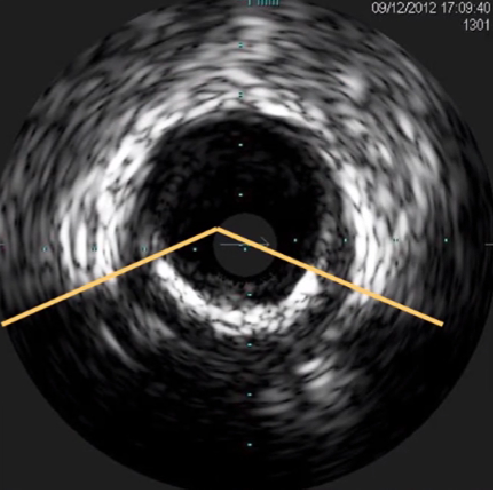
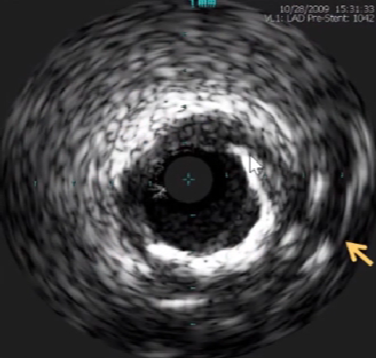
钙化斑块影像
钙化斑块后方旁伴伪影
side lobes
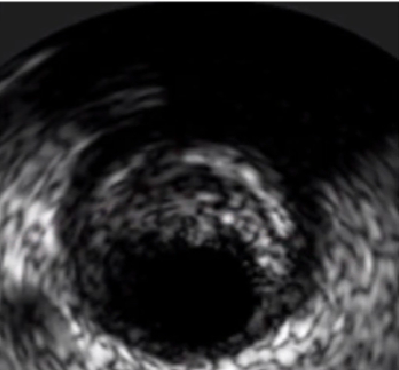
特殊斑块影像
超声衰减斑块
(破裂后无复流率高)
特殊钙化影像
钙化结节(Angio充盈缺损)
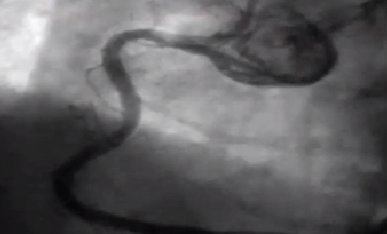
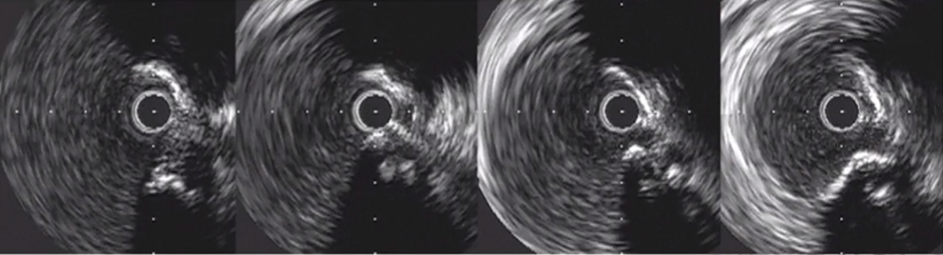
5、易损斑块
中、低回声偏心斑块,脂池形成(低回声暗区),较薄纤维帽,有或无钙化。
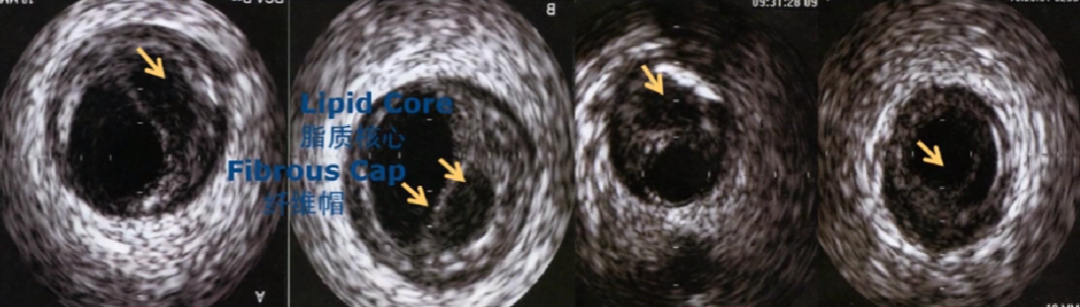
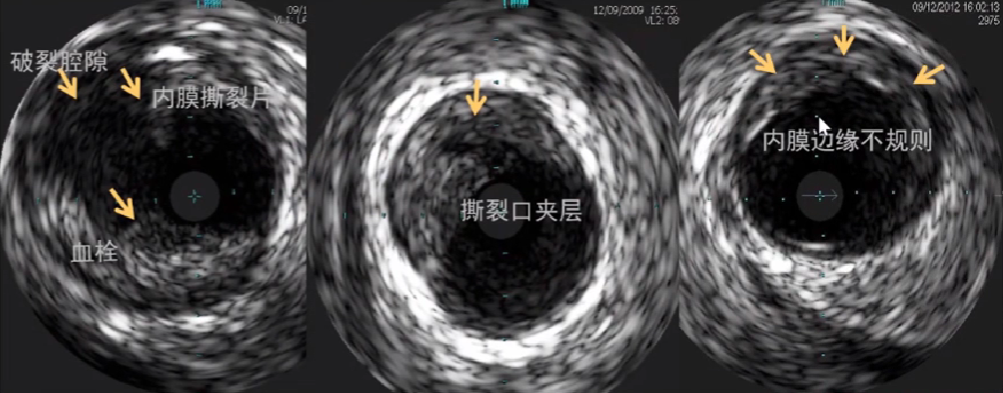
6、斑块破裂影像
内膜中断、可见撕裂片和破裂腔隙,其内有血流回声;
内膜边缘撕裂口或破溃不规则状;
伴有夹层或血栓形成。
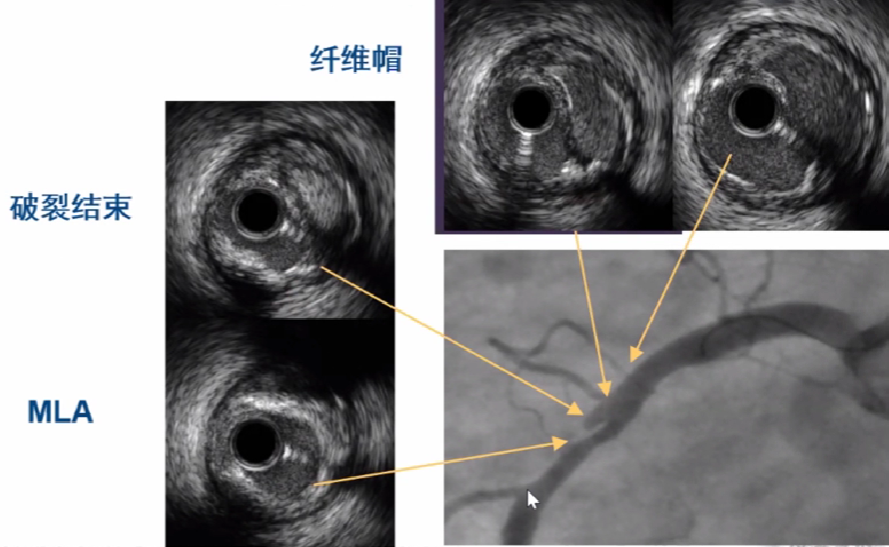
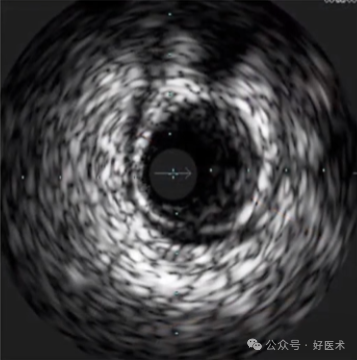
7、心肌桥影像
血管周围半月形低回声区,收缩期挤压血管,持续至舒张中晚期(挤奶现象)。
A型: 撕裂局限于内膜(斑块线形、部分撕裂);
B型: 撕裂扩展到中膜;
C型: 夹层位于斑块后方,壁内血肿形成,血管壁夹层累及范围小于180°;
D型: 血管破裂(外弹力板撕裂),血管壁夹层累及范围超过180°。
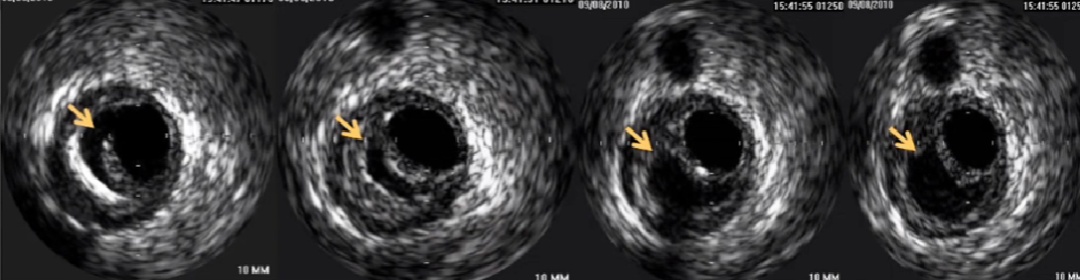
腔内不同强度的团块状回声,常有分层、分叶或带蒂状外观。血栓回声的强弱和血栓形成时间长短有关。
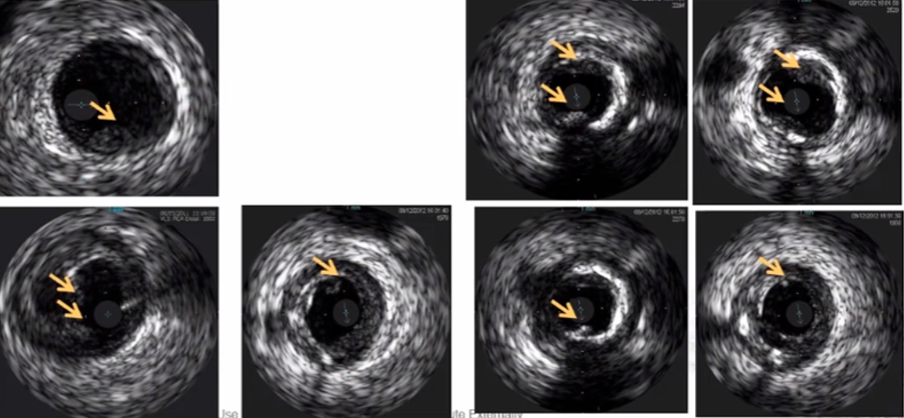
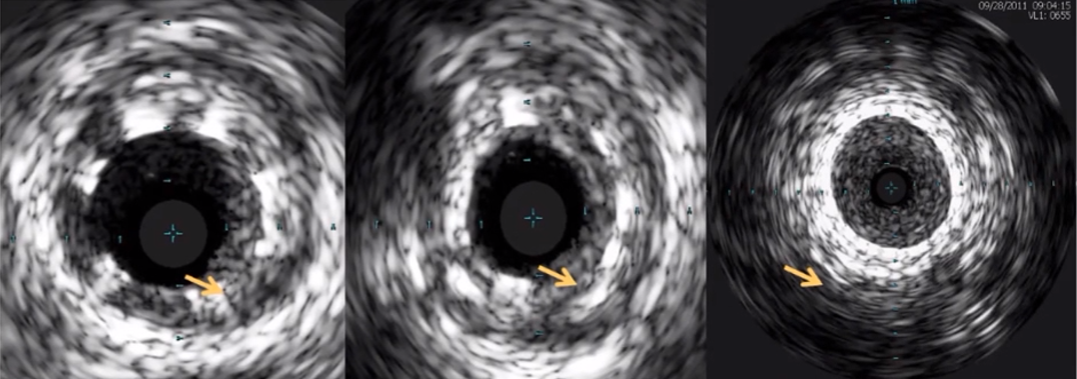
支架内膜增生, (冠脉和外周)支架内再狭隘.
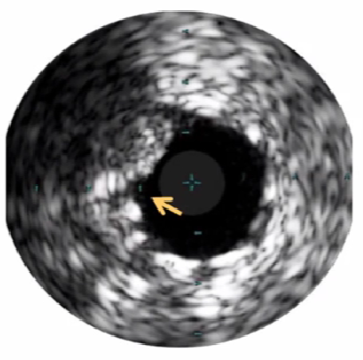
支架内组织脱垂
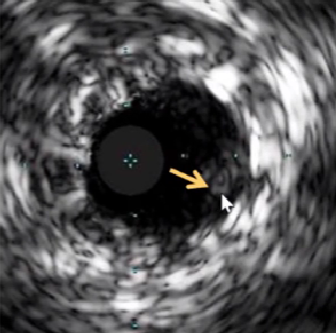
支架内血栓
8、真性动脉瘤样扩张
血管壁结构完整,血管腔面积>近端参考血管腔面积50%
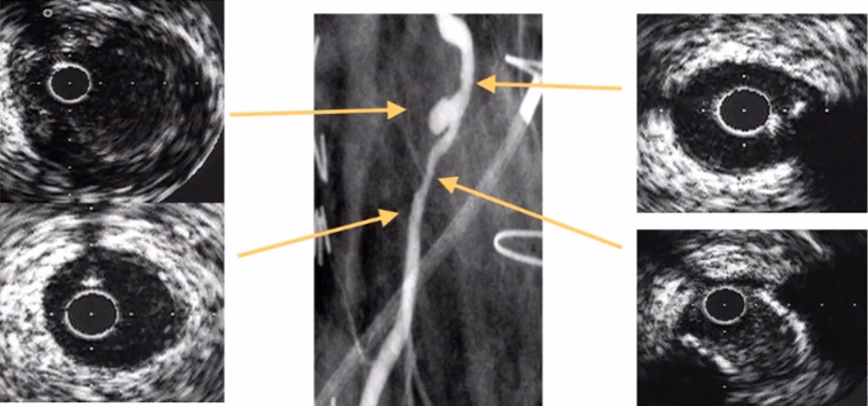
9、假性动脉瘤
管壁结构完整性丧失,伤及到外膜和血管周围组织。
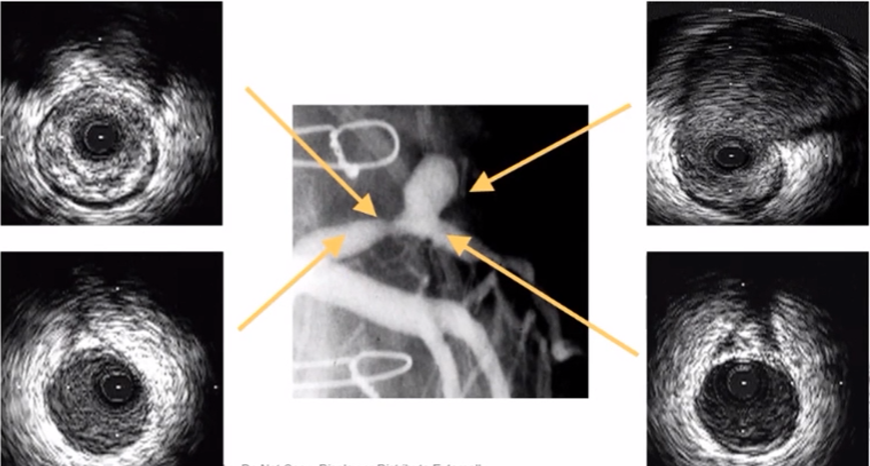
10、CTO介入治疗中超声鉴别真假腔
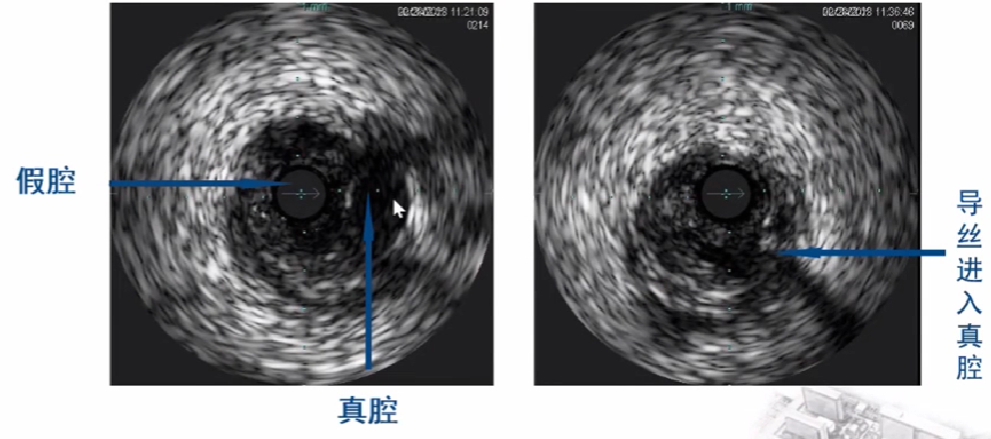
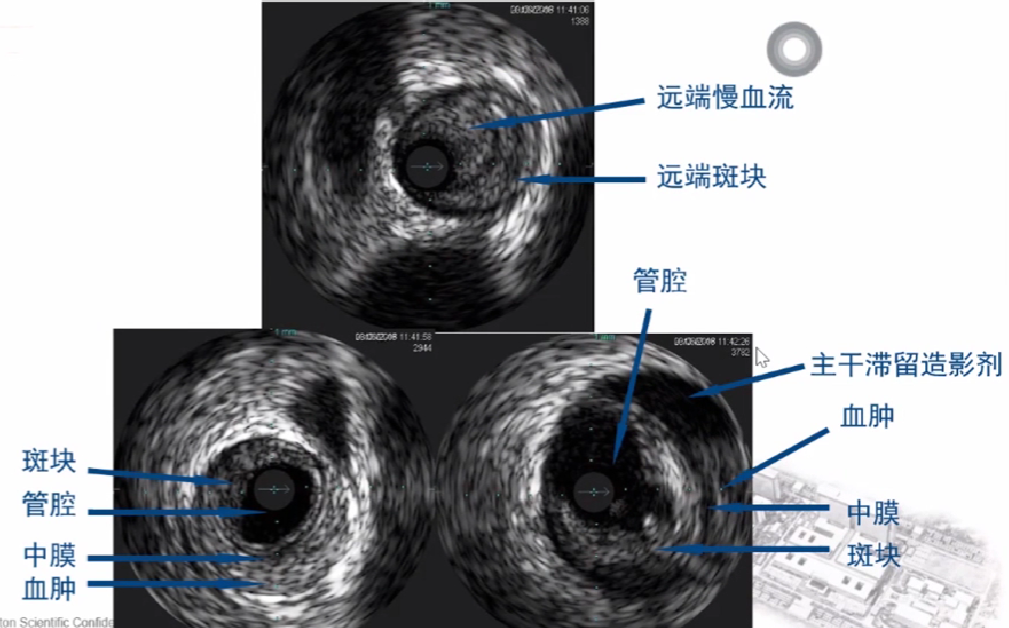
结论:
1、规范的IVUS操作是前提;
2、三层结构的识别是图像解析的基础;
3、基本概念清晰是测量的基础。
OCT图像解读及临床应用
OCT能让我们看清楚:
-
血管(三层结构)
-
纤维斑块
-
脂质斑块
-
钙化斑块
-
易损斑块
-
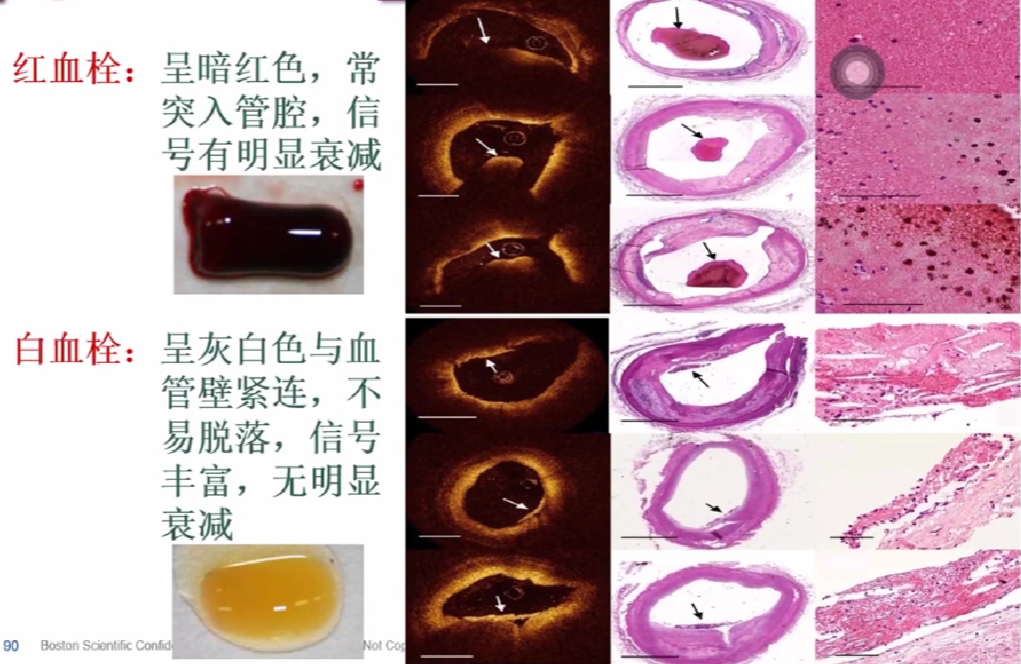
红血栓、自血栓
-
支架梁
-
支架贴壁
-
内膜增生、撕裂
-
组织脱垂
-
内膜: 单层扁平细胞+内皮下层+内弹性膜,信号丰富。
-
中膜: 10~40层环行平滑肌细胞及肌间一些弹性纤维和胶原纤维。
-
外膜: 外弹性膜+疏松结缔组织。
胶原纤维比平滑肌细胞的背向散射光强,由于外膜和内膜比中膜含有更多的胶原纤维,所以外膜和内膜的光信号强于中膜。
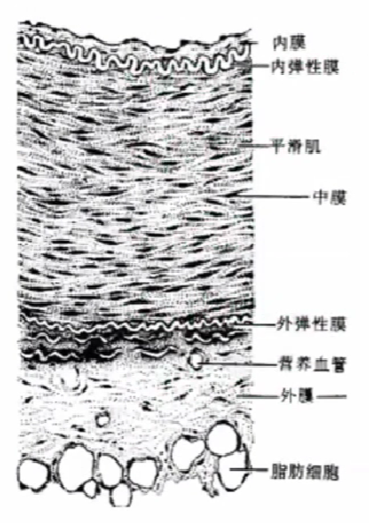
正常的血管
OCT的分辨率最高可达10um,因此可以清楚观察冠脉血管三层结构,发现异常的内膜增厚。
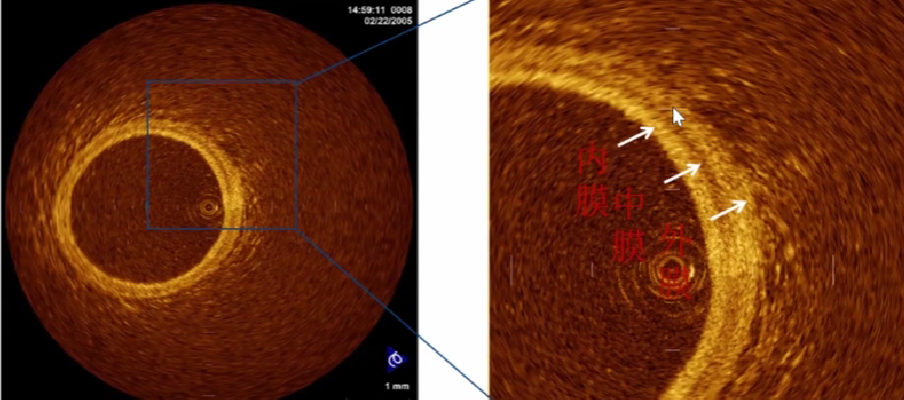
异常的血管内膜增厚
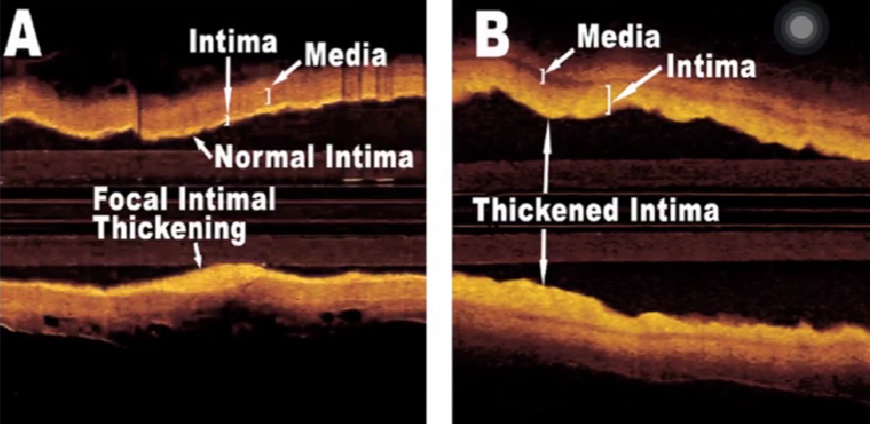
A图显示血管内膜局部增厚
B图显示血管两侧内膜均发生增殖
轻微厚型的内膜
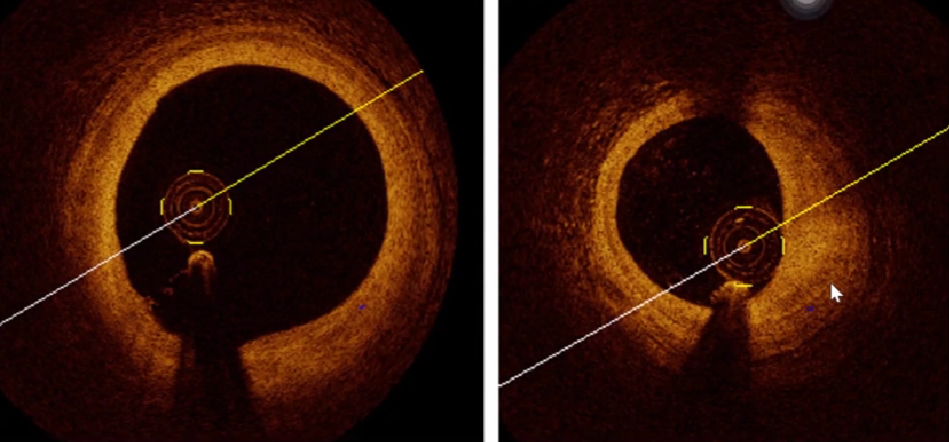
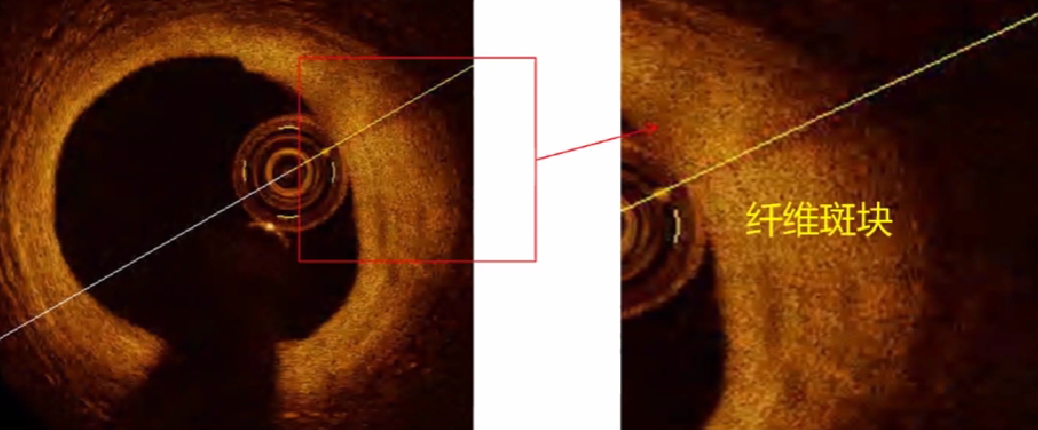
纤维斑块
纤维斑块: OCT图像显示为丰富均一的高信号区,低衰减
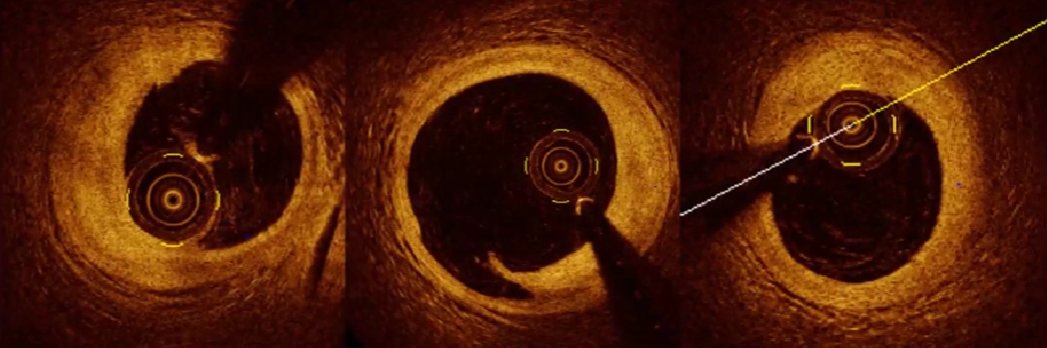
脂质斑块
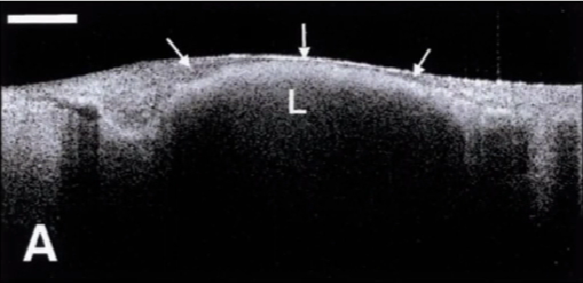
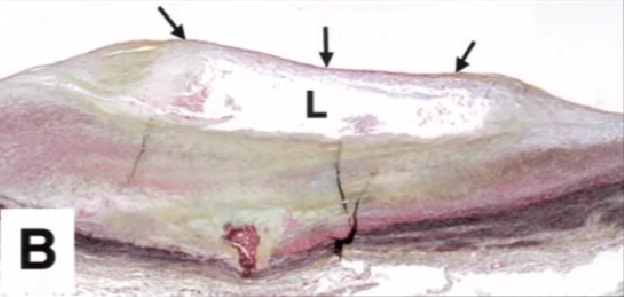
脂质斑块: 低信号区,均一,纤维帽与脂质核边界模糊,信号有衰减。

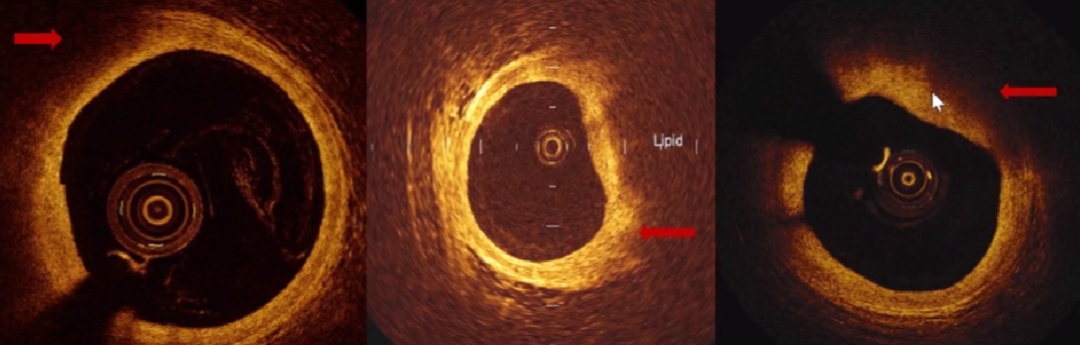
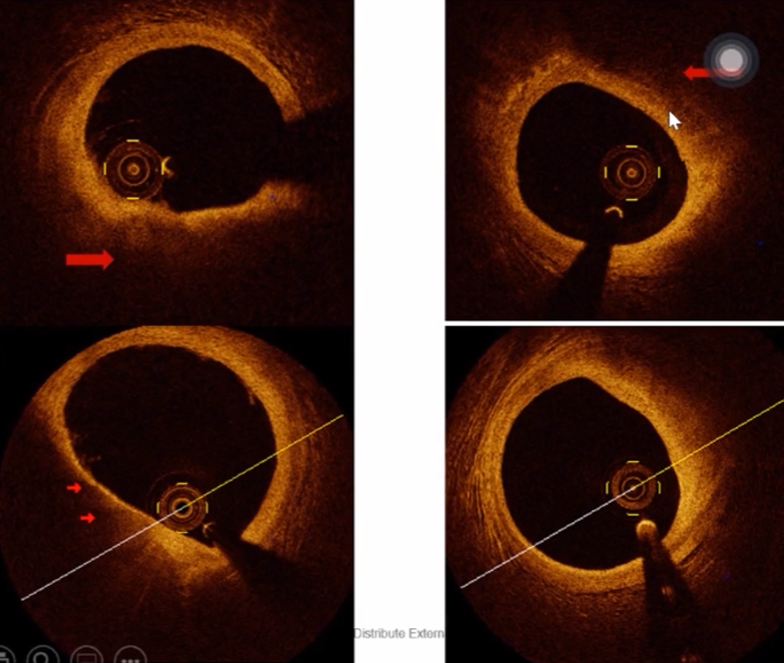
钙化斑块
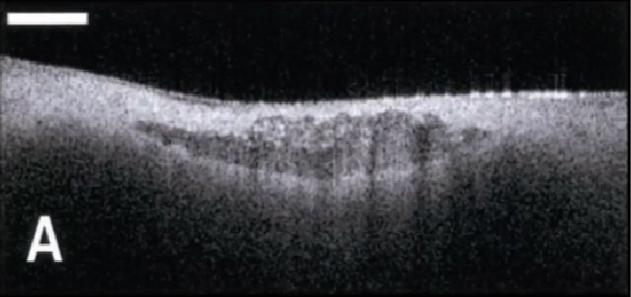
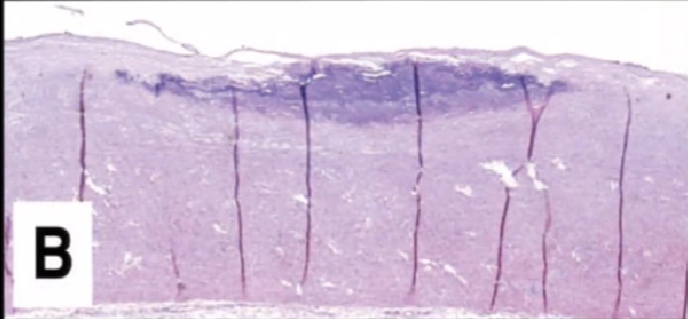
钙化斑块: OCT图像为低信号区或者异质性的区域,有清晰的边界。
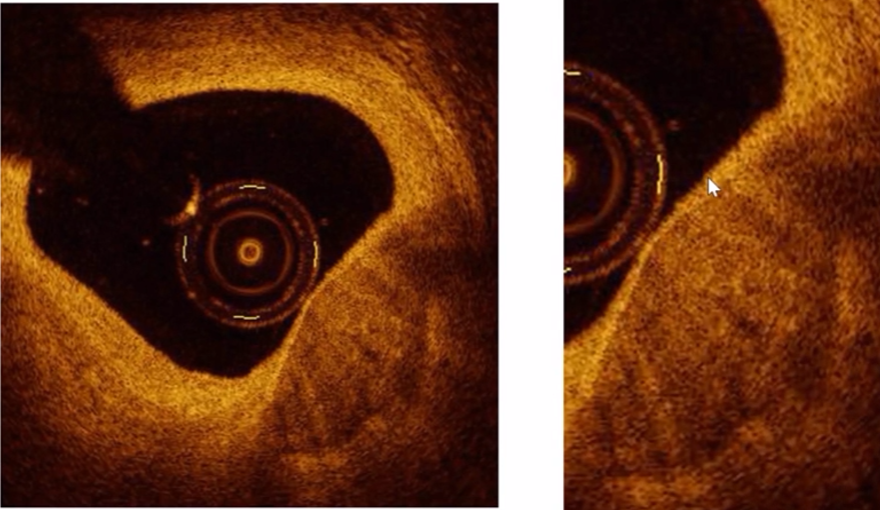
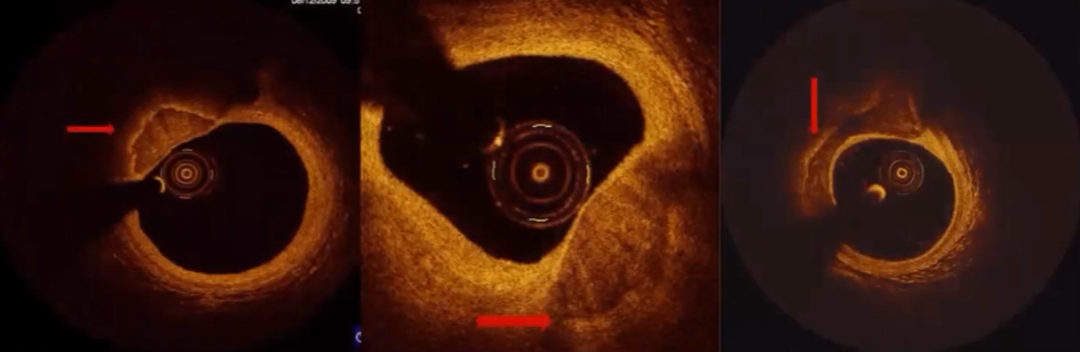
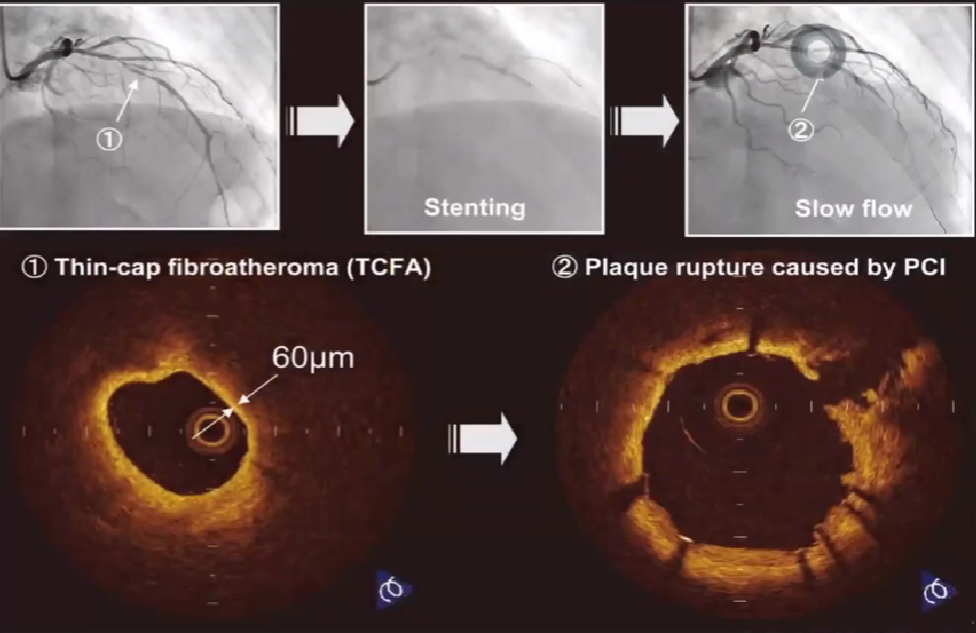
发现易损斑块(TCFA)
-
薄纤维帽(厚度<65um)
-
较大的脂质核心
-
纤维帽周围有炎性细胞浸润
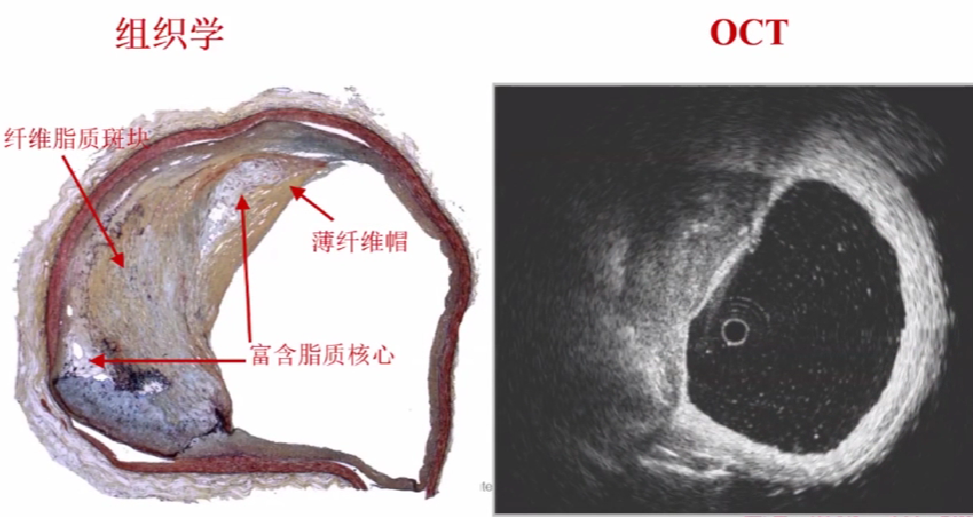
TCFA: 薄纤维帽粥样斑块
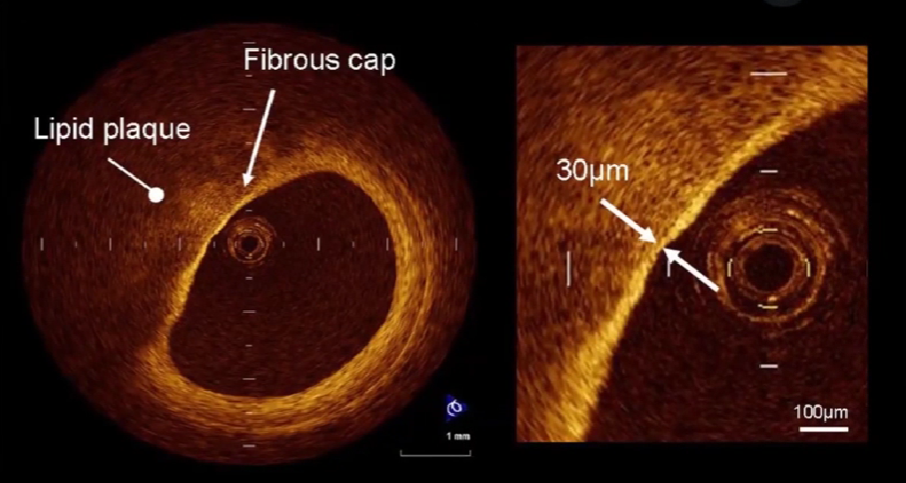
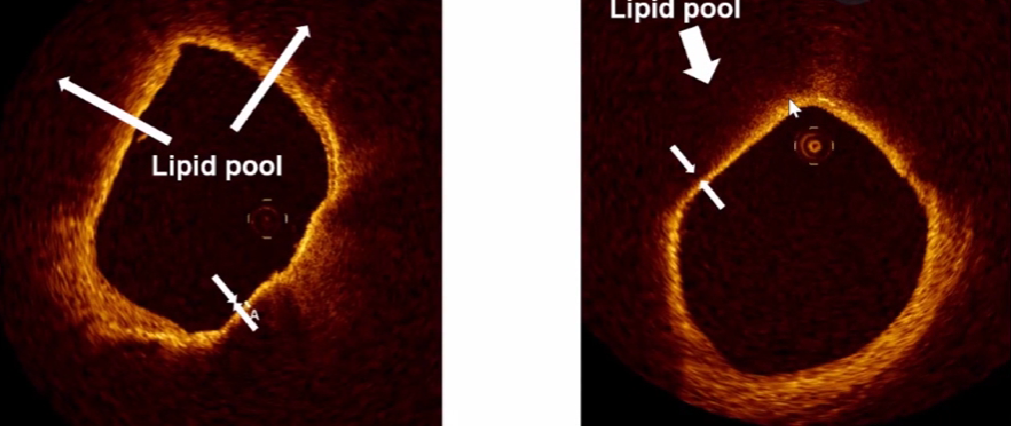
TCFA 被定义为纤维帽厚度≤65um,脂质核≥2个象限
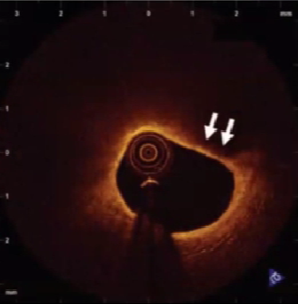
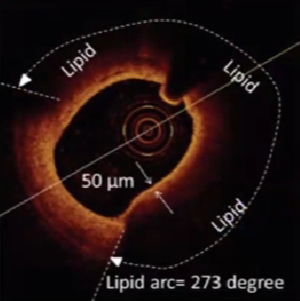
OCT能敏锐的发现斑块破裂
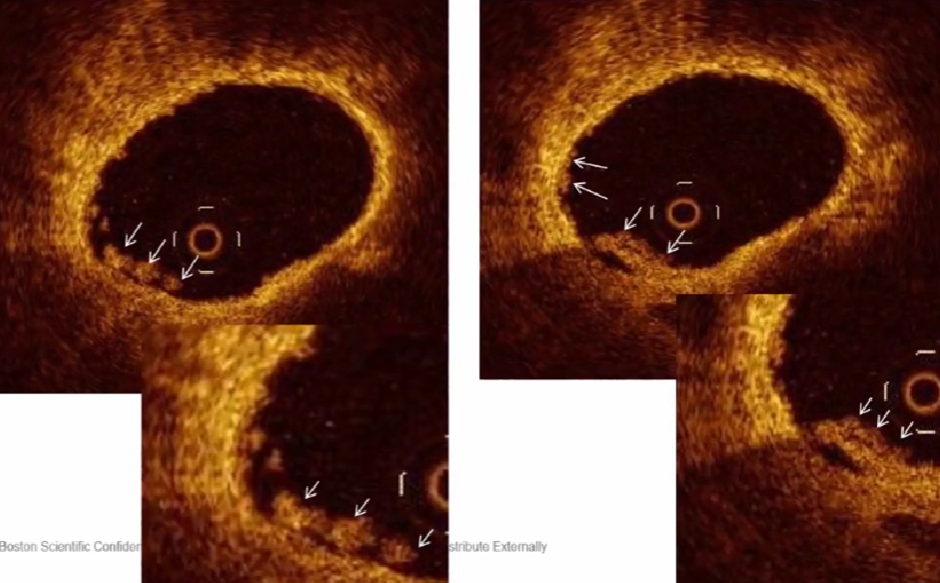
内膜侵蚀
内膜侵蚀伴表面血小板聚集
内膜撕裂
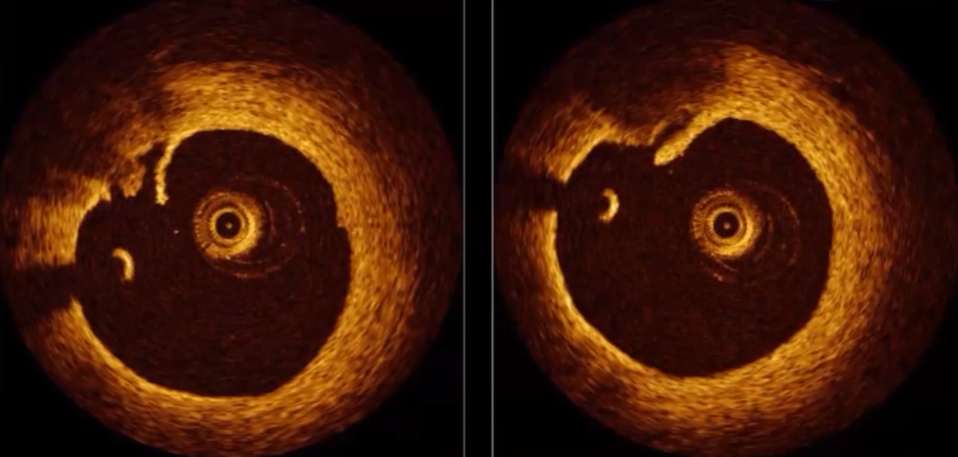
内膜夹层
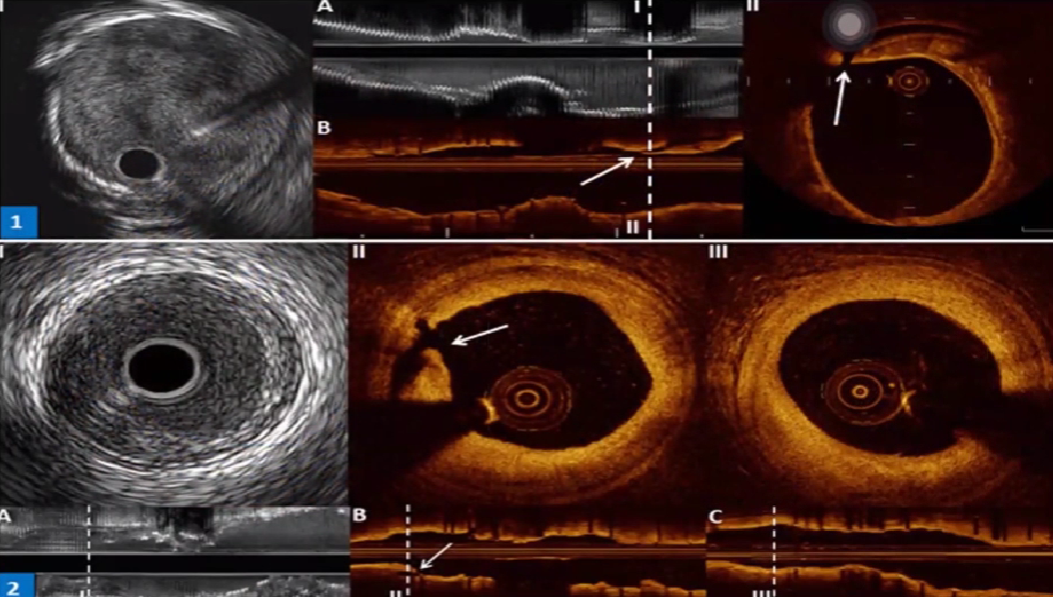
CTO:微通道
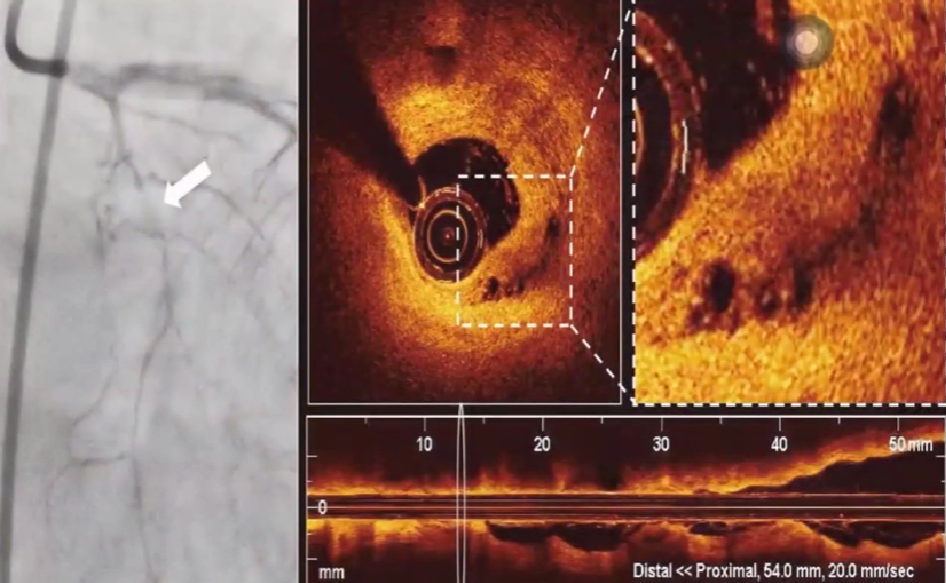
识别血栓
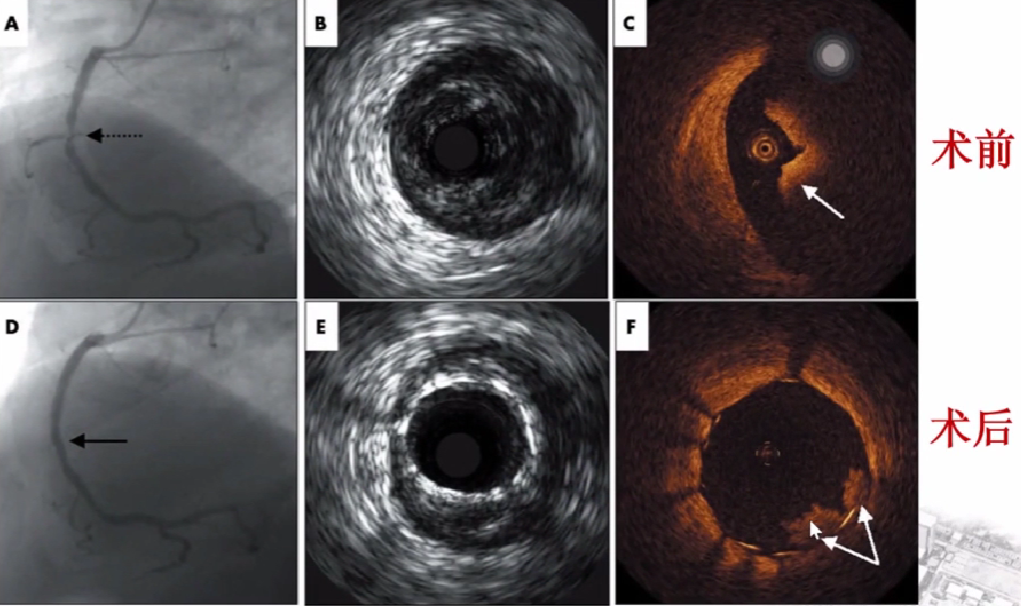
术后即刻血栓
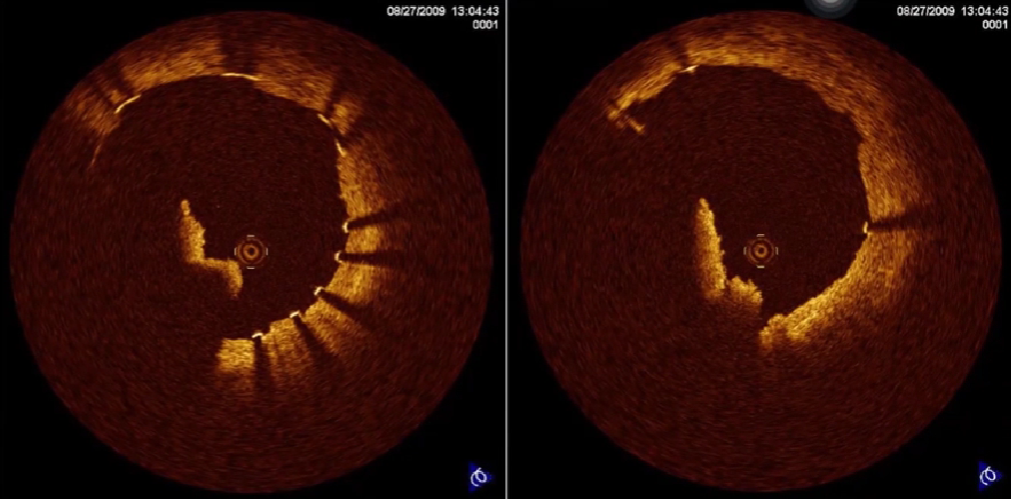
支架内白血栓
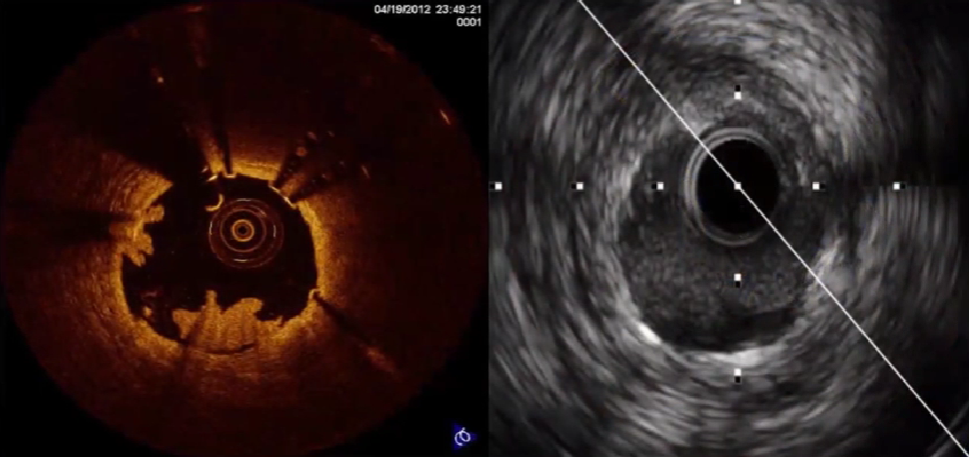
支架术后观察及随访

检查支架贴壁
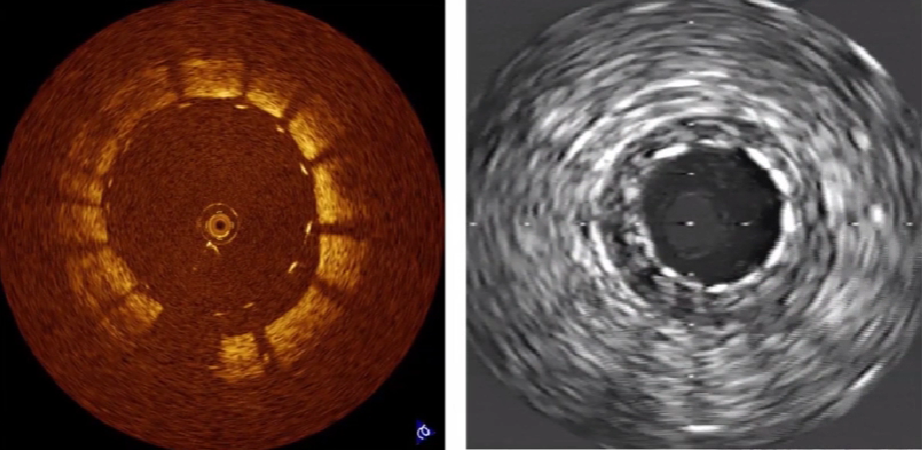
支架贴壁不良:和钙化斑块相关
检查支架植入效果
支架植入即使效果,扩张完全
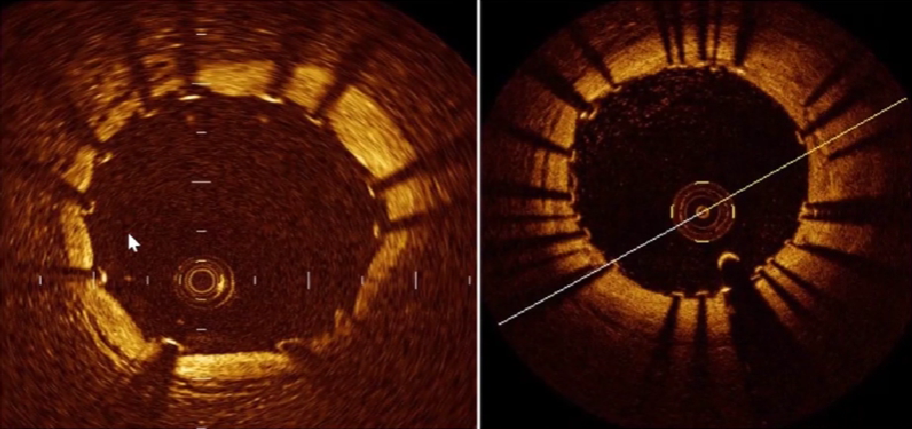
检查支架贴壁情况: 后扩后解决支架贴壁不良
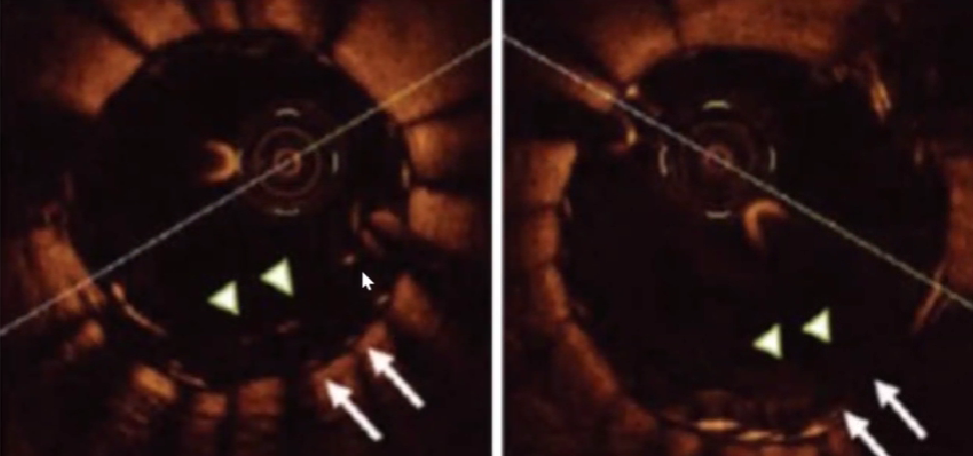
支架贴壁不良
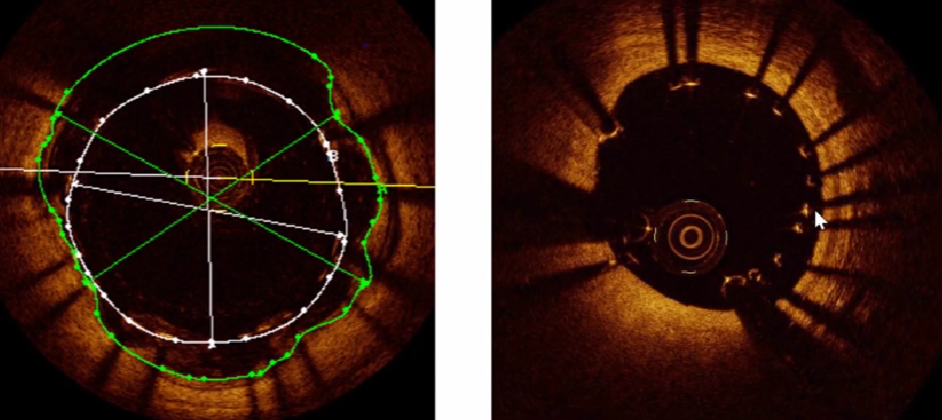
支架贴壁不良:支架梁距离内膜超过200um
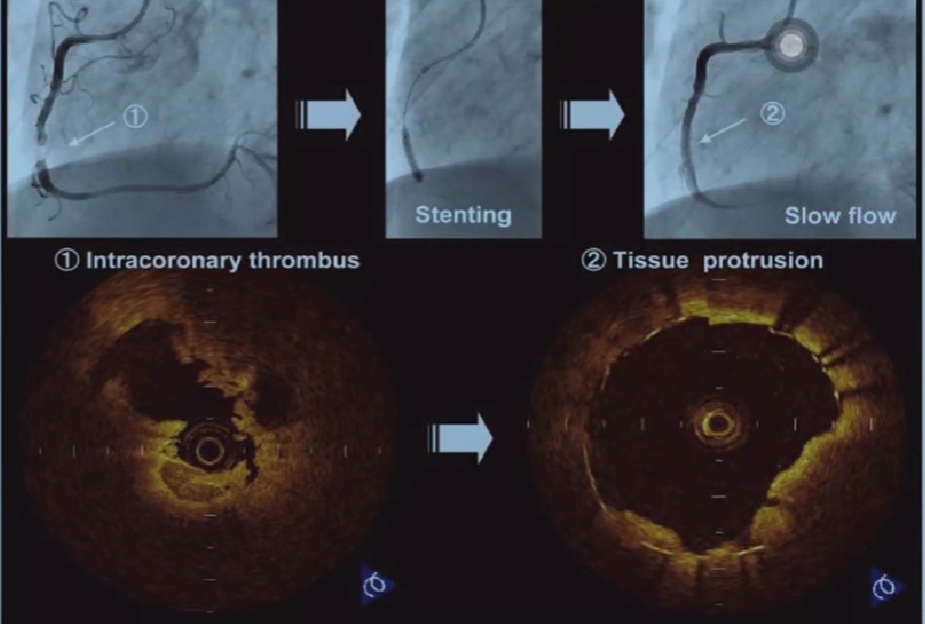
术后即刻血栓
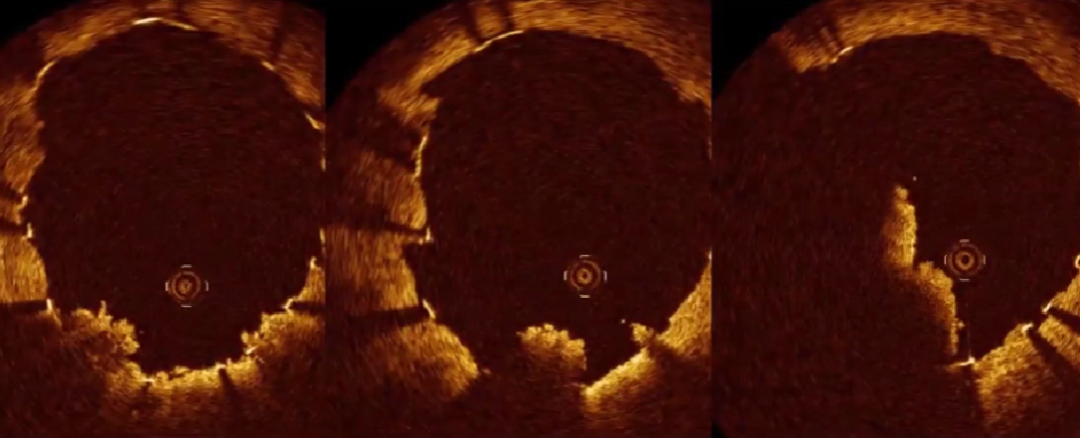
支架组织脱垂
支架后OCT发现组织脱垂
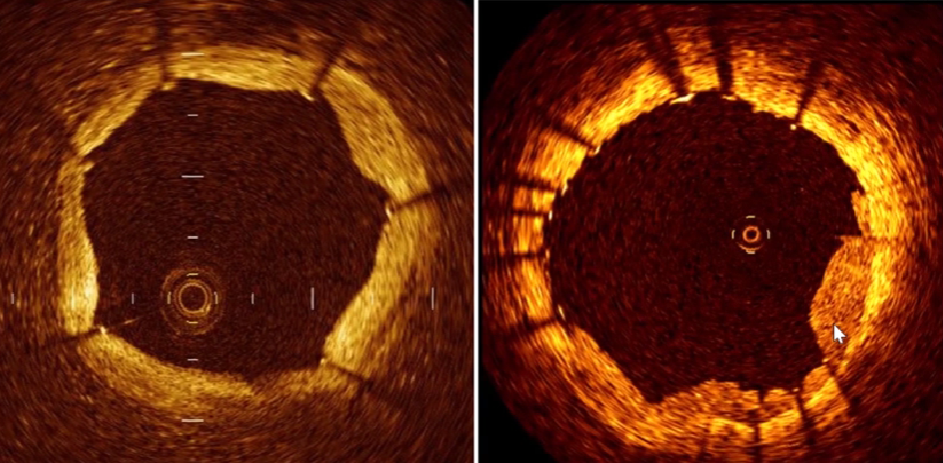
内膜覆盖良好

Matsumoto等人发现被0CT观察到的64%新生内膜没有被IVUS检测出来。
晚期支架内血栓
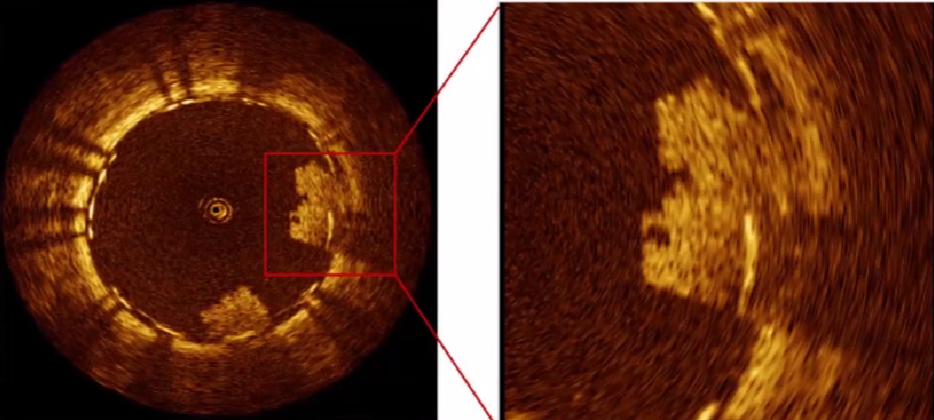
支架内再狭隘
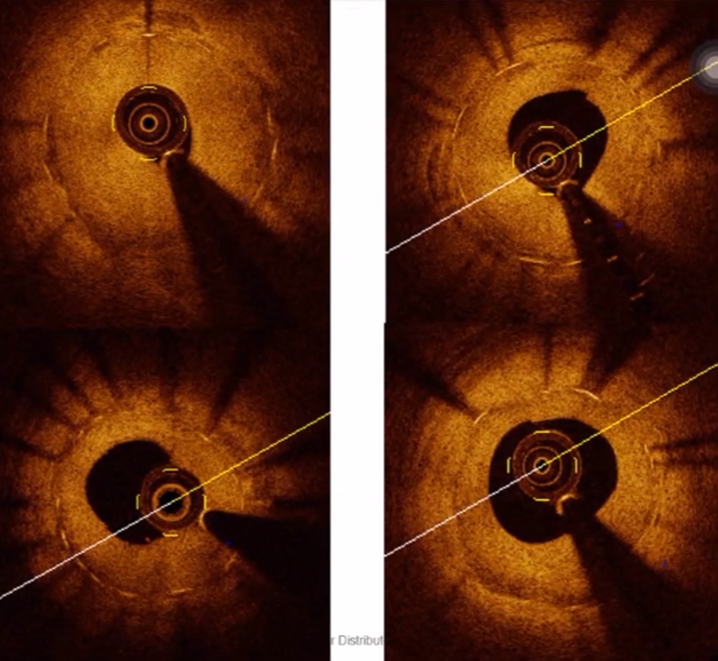
支架内钙化斑块、内膜撕裂
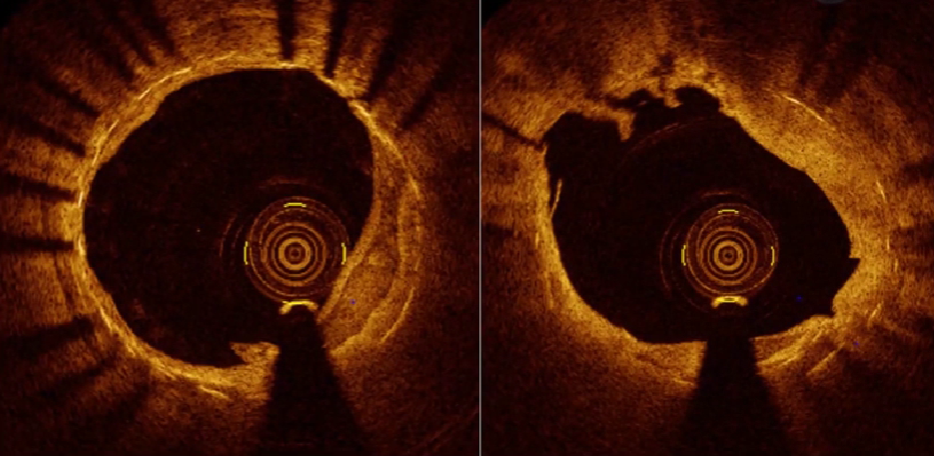
支架内不稳定斑块的破裂
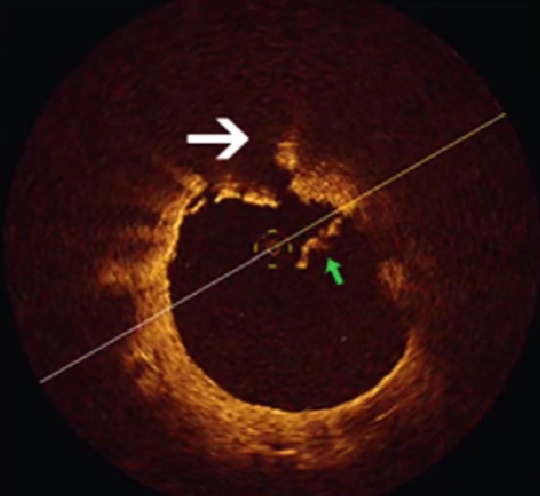
支架内不稳定斑块的破裂可能是晚期支架内血栓的成因之
正性重构
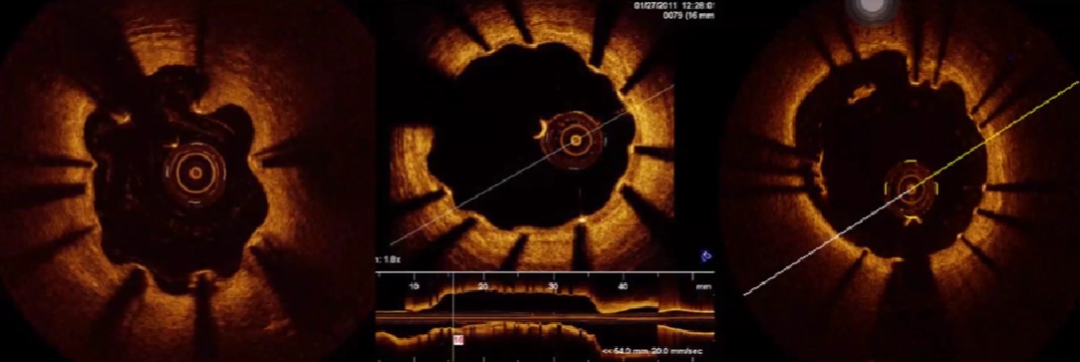
支架晚期贴壁不良
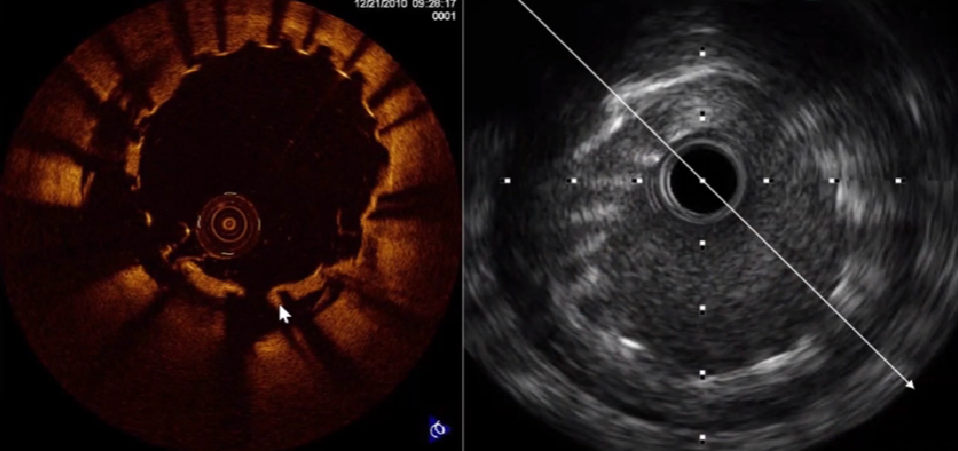
生物可吸收支架随访
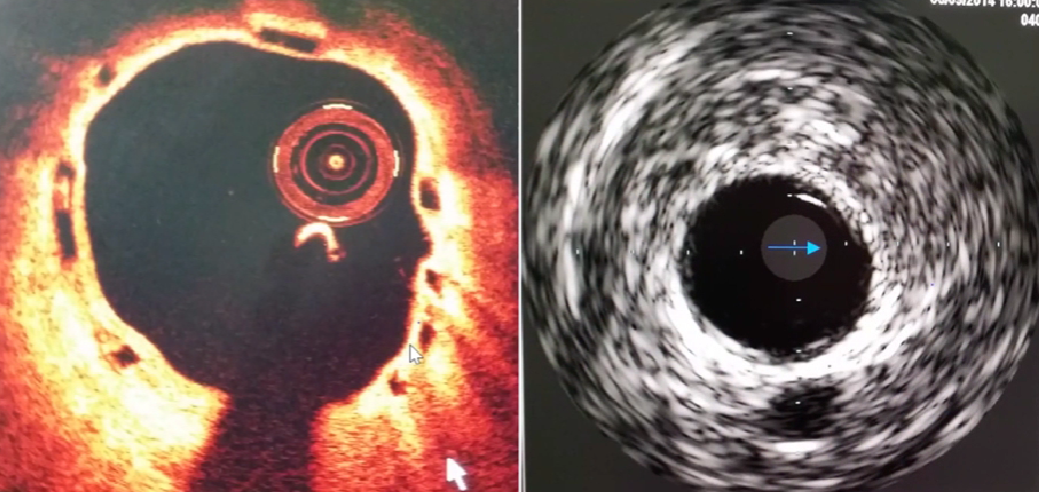
OCT的临床价值应用
-
揭示冠脉斑块形态及性质: 区分钙化、纤维及脂质斑块
-
发现易损斑块:测量薄纤维帽厚度; 发现斑块破口
-
帮助识别各种血栓:鉴别红、白血栓
-
观察支架术后即时效果:了解支架贴壁情况
-
支架术后随访:
支架内皮修复、内膜增生及血栓形成
FFR的临床应用
FFR的全称是“冠状动脉血流储备分数(Fractional Flow Reserve)”,FFR指狭窄冠脉所能达到的最大血流量和理论上不存在任何狭窄时该血管的最大血流量之比。也是在最大充血状态下,狭窄病变远端的冠脉平均压与近端冠脉平均压或主动脉压的比值。是一种用于评估冠状动脉狭窄功能意义的检查方法。FFR值小于0.8通常提示狭窄对血流有显著影响,需要进一步干预。
FFR适合用于:
-
中度狭窄的病变: 在一根或多根血管。(是否有心肌缺血)
-
连续的病变 (单根血管多处病变,罪犯病变?累积效应?)
-
弥漫性病变(压力回撤曲线,找出血流限制性病变所在部位,为点支架策略指导)
-
左主干开口或远端病变(是否有临床意义?)
-
分叉病变 (是否有临床意义?)
-
多支病变(罪犯血管?)
-
支架内再狭窄 (保守治疗?血运重建?)目前多用0CT来明确病因以指导治疗
-
先前有心肌梗死 (代替无创检查方法?)
-
STEMI患者的非罪犯病变
FFR不适合用于:
-
严重的左室肥厚患者(因其对药物的充血反应欠佳,FFR被高估)
-
ST段抬高性心肌梗死(透壁性心肌梗死<5天)
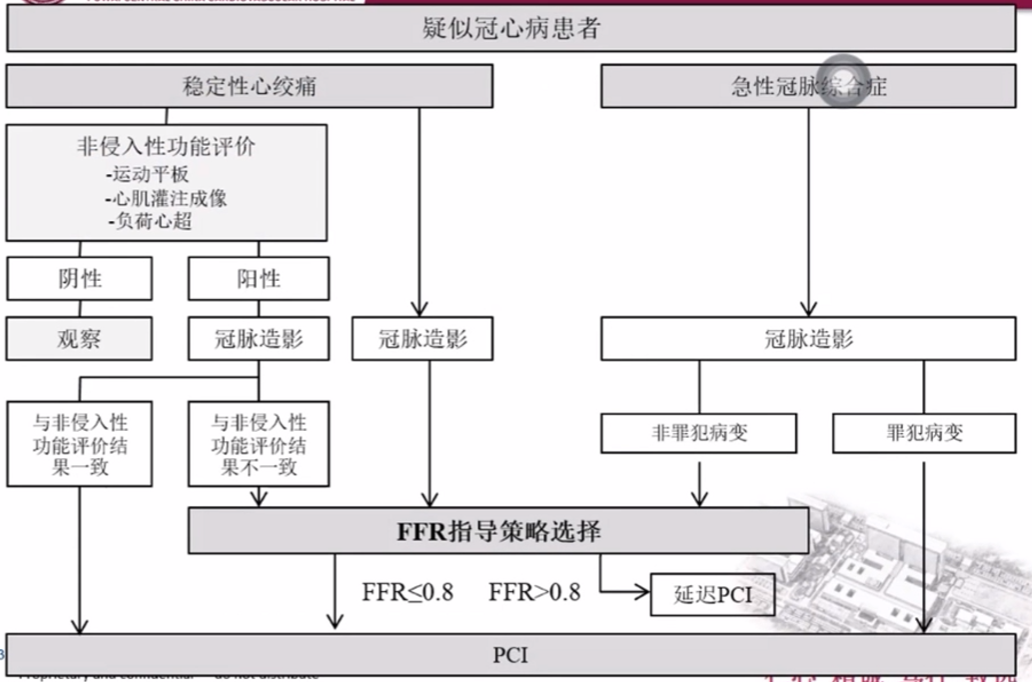
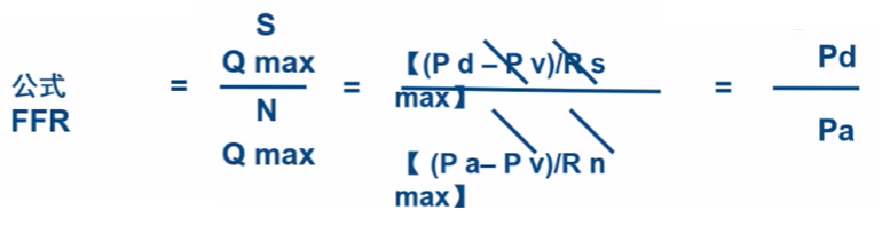
1、FFR检测注意事项
-
FFR检测不宜用于严重的左室肥厚、微血管病变,FFR值会被高估;
-
ST段抬高性心梗或心梗<5天不宜FFR检测,测值不准确;
-
中心静脉压增高有可能影响FFR值的准确性。
-
FFR检测并发症及处理同冠脉介入术;
-
术前常规应用肝素和硝酸甘油,用法与用量同其他介入操作; FFR检测前,需要冠脉内再注射硝酸甘油100 ~300ug,防止血管痉挛影响压力检测数值。
禁忌: 窦房结病变、传导阻滞、阻塞性肺病、腺苷过敏。
副作用: 患者可有类似心绞痛样胸痛,停药1~2分钟缓解,偶见窦性停搏和房室传导阻滞,冠脉用药较静脉用药更易发生。处理:停药、对症或应用腺苷受体拮抗剂(氨茶碱250mg+20ml生理盐水,5分钟内注入)。
2、FFR检测用药
1.腺苷/三磷酸腺苷: 腺苷是FFR检测基础用药。两种药物均不依赖心肌代谢需要, 通过血管平滑肌细胞腺苷A2受体产生扩张血管作用,并用量和用法相同。
a.冠脉弹丸注射:给药后10秒作用达峰,充血相持续5~15秒,30秒内作用消失,药效不稳定,部分病人不能获得最大充血状态。数分钟内可重复注射2 ~ 3次。用于非开口部位、单个病变时的局部FFR检测。
b.静脉用药: 给药后30秒起效,1~2分钟获得稳定的最大充血态,一般需持续给药3~6分钟,停药后1~2分钟作用消失。用于局部或回撤连续FFR检测,测值较冠脉团注准确,是FFR检测推荐的给药方法。
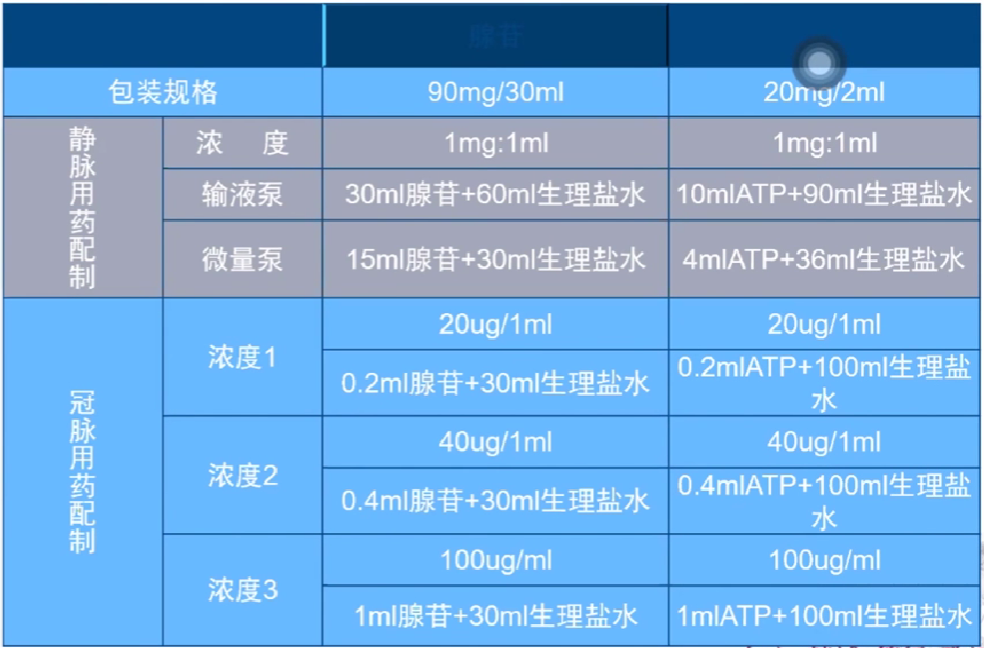
表1. FFR检测腺苷/ATP用药配制方法
表二. FFR检测腺苷/ATP静脉用药量表
*140ug / Kg/ min
根据表1 配制的浓度按公斤体重取毫升数
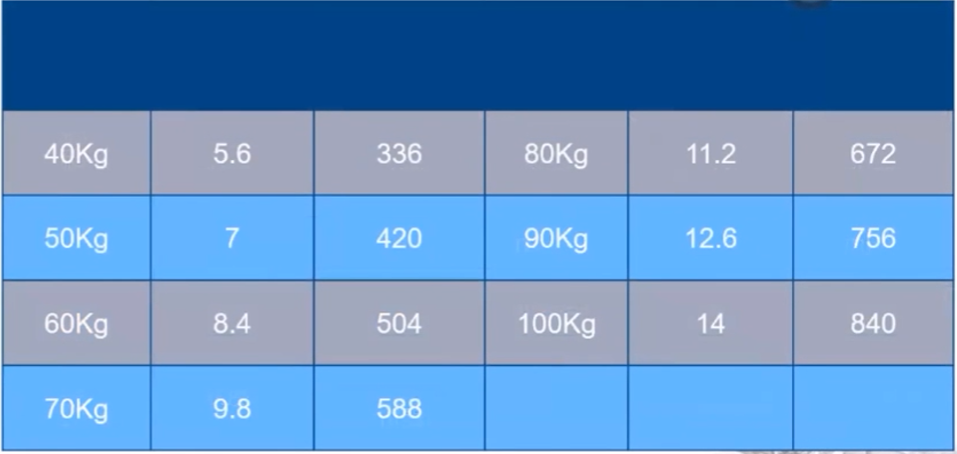
文献记载FFR检测静脉最大用药量190ug/Kg/min。
表3 FFR检测腺苷/ATP冠脉团注用量
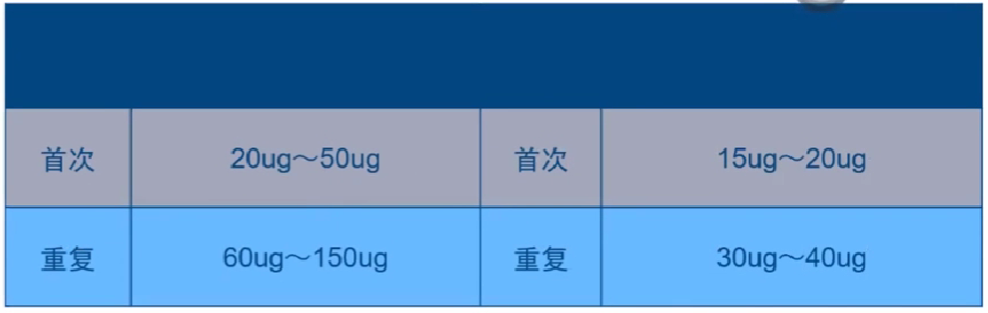
根据用药量选择表1配制的三种不同浓度之一取毫升数。
弹丸注射后,再用2~5ml生理盐水快速推注。
文献记载冠脉团注的最大剂量:左冠 200ug/次,右冠120ug/次。
3、FFR指导冠脉介入治疗
FFR用于指导冠脉介入的主要优势是可以确定缺血相关血管和缺血相关病变。1.多支血管病变、2.左主干病变、3.分叉病变、4.长病变和多处病变、5.临界病变、6.评估介入治疗预后。7.FFR检测对评估是否外科搭桥具有重要意义。
FFR是目前心导管室评估冠脉病变功能意义的金标准。冠脉内FFR检测简单、安全、快捷,FFR指导治疗的病变具有更好的临床疗效同时可减少造影剂用量,并以较低的成本改善预后。
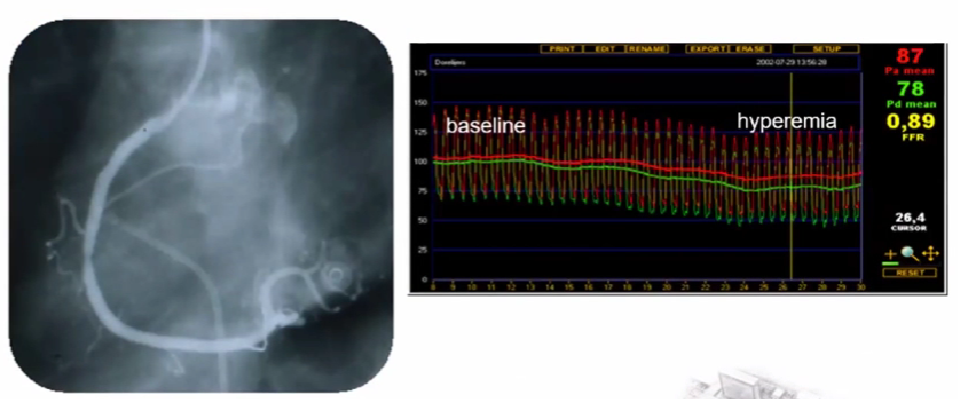
FFR的临床应用---临界病变
中度狭隘病变(50%~70%)
FFR的临床应用---多处病变
同一血管多出病变
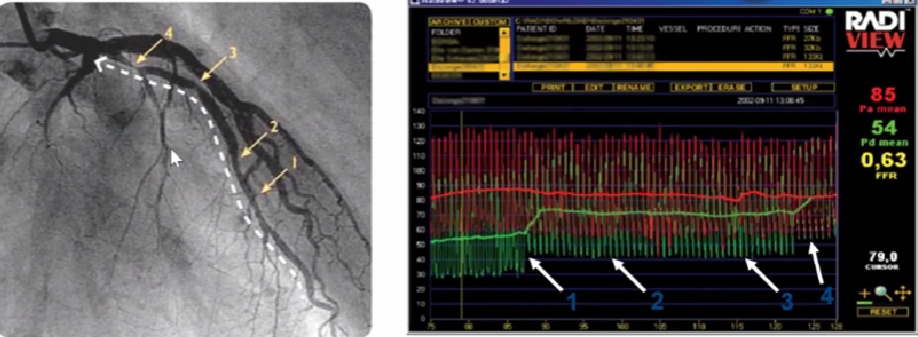
通过对病变进行压力回撤,可以识别出“罪犯”病变。
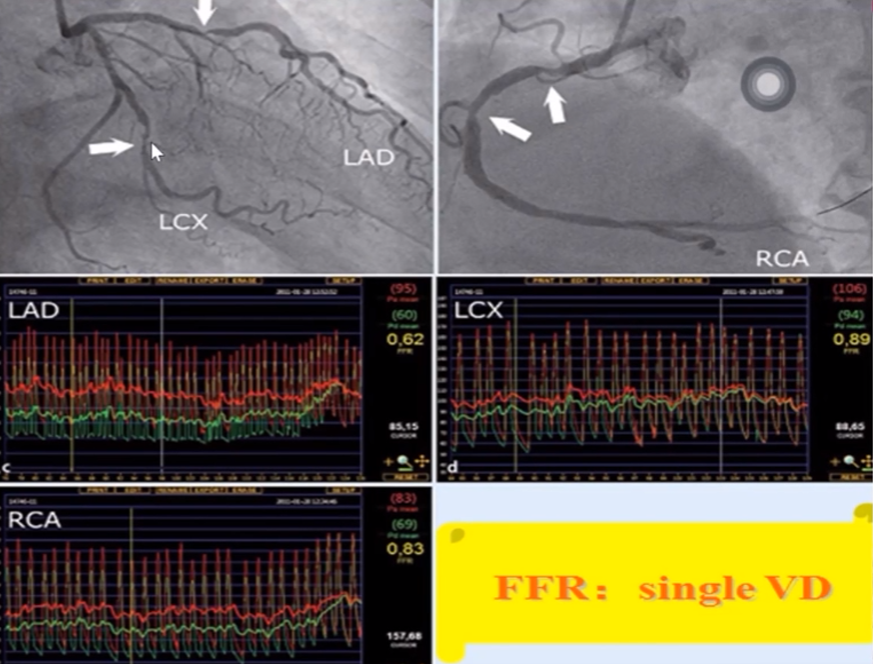
FFR的临床应用---多支血管病变
FFR的临床应用---弥漫病变
通过压力回撤来识别罪犯病变或者揭示血管中的弥漫性病变的情况。
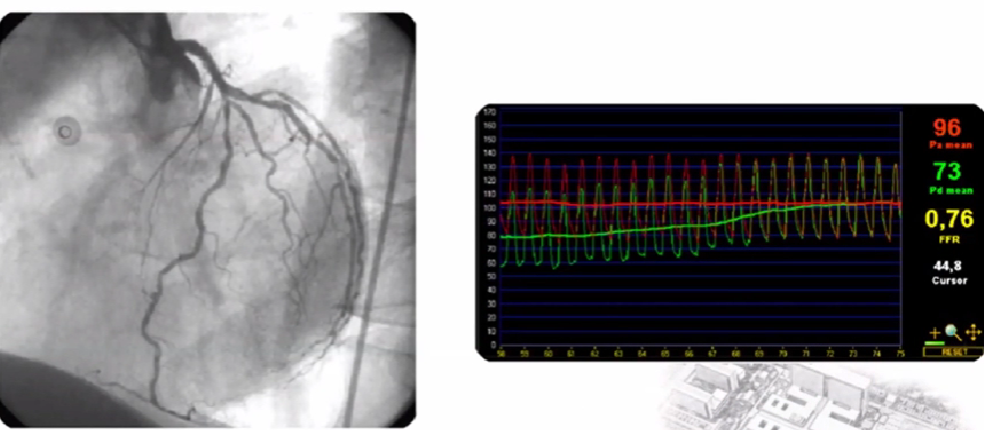
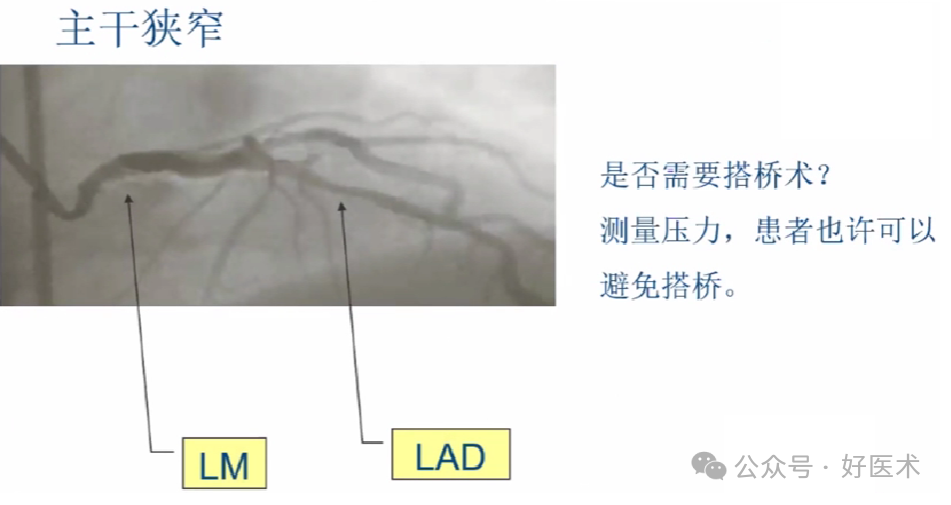
FFR的临床应用---左主干
-END-
声明:以上图源均来源于<好医术经典课>,课程讲师:华中阜外医院郑晓晖,内容仅代表作者个人观点,仅用于学习交流,望大家理性判断及应用。













