
经皮椎体后凸成形术( percutaneous kyphoplasty PKP)在全球范围内广泛用于微创治疗骨质疏松性椎体压缩骨折( osteoporotic vertebral compression fracture,OVCF),取得了显著的临床疗效。截止2016年12月,我国共有1443家医院在330本杂志报道约73992例次接受PKP手术治疗。该技术在影像引导下经皮穿刺置入球囊扩张后将骨水泥注入骨折椎体内,使病椎即刻得到强化和稳定,恢复其负重功能,迅速缓解患者疼痛,明显改善生活质量,得到医生和患者的广泛认可。虽然PKP手术疗效令人满意,但其手术的高风险性仍不容忽视。骨水泥渗漏、肺动脉栓塞等并发症不仅会造成脊髓神经损伤、瘫痪,甚至危及生命。在术前诊断,术中穿刺、复位、灌注,术后处理等方面仍存在相关问题有待解决。为此,临床医师应重视PKP手术的规范化操作,掌握PKP手术应用过程中常见问题的处理策略,降低手术并发的发生率,提高手术疗效。
一
术前
(一)诊断
结合患者年龄、病史、症状、体格检查、影像学检查和骨密度测定等临床资料明确OVCH的诊断,仔细排除脊柱非特异性感染、结核、肿瘤、低磷血性骨软骨症等疾病。同时,对患者的手术耐受性进行评估,严格掌握手术适应证。当怀疑脊柱非特异性感染、结核时,不可行PKP手术治疗,需明确诊断后再做处理。对于脊柱三柱均累及的骨折,也不适合PKP手术。
(二)疼痛责任椎体
术前必须精确判定OVCF疼痛责任椎体。对于多节段椎体压缩患者,术前应确定哪些节段的压缩椎体可导致疼痛;对于单椎体压缩骨折病例,也应明确疼痛是否来源于该椎体。这些引起疼痛的骨折椎体即为疼痛责任椎体,也是手术目标椎体。疼痛责任椎体的判定需结合患者的症状、体格检查及MR检查,即:患者有明确的腰背痛症状;体格检查相应节段有压、叩痛;MRI显示相应节段椎体内有信号改变,常见椎体内有水肿信号,表现为T1加权像低信号、T2加权像高信号或等信号及脂肪抑制序列成像高信号,而对于椎体内含气体改变者,可表现为低信号。MRI检查有禁忌证者,可行核素骨扫描,表现为相应节段核素浓集。
OVCF患者骨折愈合能力差,易发生骨折不愈合,以往对此类疾病认识不足,易漏诊误诊。文献报道OVCF骨不愈合发生率约10%左右。此类疾病常具有如下特点:无明显外伤史或仅有轻微外伤史,伤后出现持续数周至数月的腰背部疼痛,脊柱承载负荷或改变体位时疼痛加重;查体发现脊柱受累节段的叩击痛;CT或MRI上可见椎体内“真空征”或“裂隙征,动力位X线片可见椎体内存在异常活动,有假关节形成。结合上述的病史、体征及影像学检查,不难诊断OVCF骨不意合。OVCF骨不愈合患者的治疗有其特殊性、常规的PKP手术方法难以获得满意疗效。
二
术中
(一)体位
可选用局部麻醉或全身麻醉。常规采用俯卧位。极少数患者由于肋骨骨折,肋软骨炎导致前胸壁疼痛,或者因为心肺功能不好,不能耐受完全俯卧位时,可根据具体情况采取其他相应体位,如侧卧或侧俯卧位,但须注意侧卧或侧俯卧位时术中患者可能改变体位影响穿刺。
(二)穿刺
1.术前定位:采用“一线影”基准定位法,在穿刺操作前调整X线球管的投照方向,使骨折椎体的终板呈“一线影”,即骨折椎体的上/下终板在正侧位X线透视像上呈一直线,并且两侧的椎弓根影在正位透视像上以棘突为中心的对称分布,在侧位透视像上完全重叠(图1)。穿刺前对骨折椎体进行透视下定位,确定合适的穿刺点和穿剌路径,避免X线投照偏差造成穿刺失败。
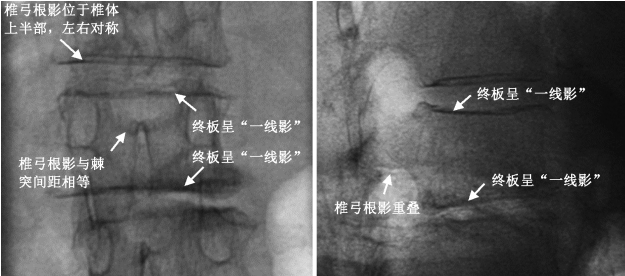
图 1 X 线正侧位投射下病椎终板成像为一直线
2.穿刺路径:OVCF椎体前柱通常压缩明显,PKP经球囊扩张复位骨折,但扩张的球囊不能撑破椎体周壁骨质,故术前要根据骨折类型及压缩程度设计好穿剌路径。在胸椎穿剌时可采用经椎弓根外途径穿刺,经肋-横突之间在椎弓根根部与椎体移行处穿入椎体。如果穿刺内倾角过大,穿刺针进入椎管损伤神经脊髓的风险加大,过小则导致球囊过于偏在椎体一侧,球囊扩张可能导致椎体周壁骨折。穿刺过程中,椎体尾傾角变化较小,内角变化较大。T4~T8椎体通常选择择经椎弓根外途径穿剌,T9~L1椎体通常根据该节段椎弓根横径的宽度和内角度选择椎弓根外或者经椎弓根途径穿刺,L2~L5椎体多选择经椎弓根途径穿刺。
3.穿刺过程:以经双侧椎弓根穿刺途径为例。在正位N线透视下,首先将穿刺针尖置于双侧椎弓根的外上缘,左侧为10点钟、右侧为2点钟的位置,根据不同手本节段和骨折类型,进择恰当的穿刺点和穿刺方向,缓慢地锤击穿刺针。当正位透视穿刺针针尖位于椎弓根影的中线时,侧位透视穿刺针针尖应该抵达椎弓根影前后径的1/2。继续锤击进针,当正位透视穿刺针针尖接近椎弓根影的内侧缘时,侧位透视针尖应抵达椎体后壁,然后继续进针2-3mm,完成穿刺(图2)。
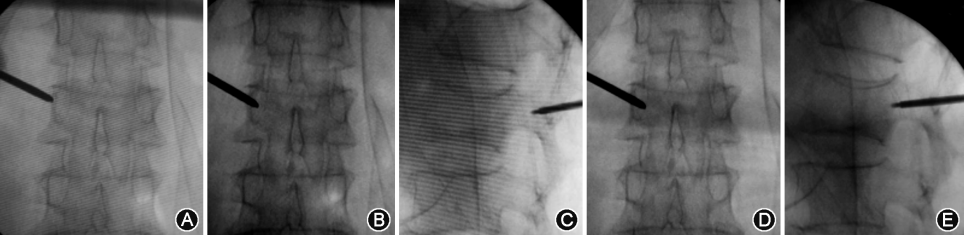
图 2 经双侧椎弓根穿刺 X 线图:A 显示左侧穿刺点为 10 点钟位置;B 正位显示穿刺针尖位于椎弓根影的中线处;C 侧位显示针尖位于椎弓根影的 1/2 处;D 正位显示穿刺针尖到达椎弓根影的内侧缘;E 侧位显示针尖到达椎体后缘。
若OVCF患者骨质疏松严重,合并退行性侧弯,或者骨折节段位于中上胸椎,使得C型臂透视影像不清晰,甚至无法取得标准的椎体正侧位影像;有条件的医院可在计算机辅助导航下进行穿刺,通过术前合理的路径规划和术中实时的穿刺路径监测,使其穿刺成功率显著提高,以提高手术安全性。穿刺完成后,进行术中CT扫描确认穿刺针位置正确后,仍需要在X线实时监控下完成球囊扩张和骨水泥灌注。
(三)复位
1.置入球囊:穿剌完成后,取出穿刺针的内芯,插入导针,然后拔出穿刺针,沿着导针的方向依次插入扩张套管和工作套管(避免导针跟进穿出椎体)。骨锤缓慢锤击,当工作套管的头端达到椎体后缘皮质前方2-3mm时,将精细钻置入工作套管中,使用手指的力量按照顺时针的方向将其缓慢地钻入椎体,当侧位透视像上显示钻头尖已到达距离椎体前缘5-10m时,依然顺时针方向旋出精细钻。使用带芯的骨水泥推杆将骨道夯平,然后置入可扩张球囊,球囊的位置应该放在椎体的前中部,置于塌陷终板的下方或者距离椎体上下终板相等的位置(球囊的放置部位取决于穿刺入路)。这样不仅可使终板恢复高度,面且降低了球囊撑破椎体终板的风险,减少骨水泥椎间隙渗漏的发生率。另外,利用球囊在椎体的前中部扩张空腔,使空腔与椎体后缘皮质间留有骨质间隔,从而降低骨水泥向后渗漏的风险。
2.扩张球囊:扩张球囊的速度应缓慢进行,当压力达到50psi时,拔出球囊的内芯以继续扩张。为避免球囊破裂,压力原则上不应超过300psi,球囊内造影剂液体量不超过3ml。在实施球囊扩张前必须排尽球囊内的空气,否则影响球囊显影。球囊内所用的造影剂应选用不透血脑屏障的造影剂,如碘海醇(欧乃派克),不可使用可透血脑屏障的造影剂,如泛影葡胺。球囊停止扩张的指标:骨折已复位;球囊与椎体周壁皮质或终板接触;球囊达到最大压力;球囊达到最大容积。球囊扩张及复位满意后将可扩张球囊复原后撤出。
(四)灌注
1.骨水泥初始注入时间点:将调制后的骨水泥放入推管中,术者每隔数秒钟使用橡胶手套接触推管口的骨水泥,将骨水泥刚好不粘橡胶手套的时刻(骨水泥拉丝期后期)作为骨水泥初始注入的时间点(“不粘”始注技术)。该时期的骨水泥在椎体中不仅能够充分弥散,而又不容易渗漏至椎旁血管中,进而降低骨水泥肺动脉栓塞的风险。
2.灌注方法:骨水泥灌注遵循在术中实时动态透视监测下从前向后灌注的原则,适时、间隔、低压地灌注骨水泥。为降低骨水泥渗漏风险,应掌握以下骨水泥灌注技术:(1)温度梯度灌注技术。椎体内温度与手术室温度存在温度差,骨水泥在高温椎体内(37℃)的凝固速度比低温手术室内(20℃)快。当灌注的骨水泥弥散至骨折椎体的破损周壁时,暂停灌注骨水泥,由于手术室的温度低于椎体内的温度,椎体内的骨水泥凝固快于体外,待椎体破损周壁处的骨水泥稍凝固后,再继续缓慢灌注体外未凝固的骨水泥,利用这一特性,在保证骨水泥充分弥散的同时,降低了骨水泥渗漏率。(2)二次调制灌注封堵技术。对于伴有椎体前壁和前侧壁破裂或缺损的椎体,首次推注小剂量团状期中晚期的骨水泥以封堵椎体周壁的破裂或缺损区,待椎体内骨水泥接近凝固后,将拉丝后期骨水泥继续推注入椎体,不仅可以降低骨水泥渗漏率,而且可使骨水泥与椎体锚合牢固,防止骨水泥整体脱出。
3.骨水泥灌注量:骨水泥注入量应根据椎体大小,骨折类型和压缩程度等而定。对于重度压缩性骨折的椎体,建议双侧穿刺入路,并适当减少骨水泥量,降低骨水泥渗漏风险;灌注骨水泥的体积应稍大于球囊扩张的空腔容量,以完全充填椎体内空腔并弥散至空腔周围骨小梁内为宜。当发现骨水泥有渗漏倾向或抵达椎体后1/3时应立刻停止灌注。对于重度骨质疏松的患者,灌注骨水泥的量过少或者分布不均匀,术后可能出现手术椎体或邻近椎体的再骨折。骨水泥灌注完成后,将带内芯的骨水泥推杆置人工作通道中,与通道管口平齐,避免骨水泥向外渗漏。观察3-5min,等待骨水泥完全凝固后方可取出工作套管。
4.常见并发症的处理:骨水泥椎管内渗漏,若无明显神经症状,可予以观察,不需特殊处理;若出现骨水泥压迫脊髓症状,尽早使用激素、脱水药物,减轻脊髓水肿,防止继发性损伤,同时行CT或MRI检查明确压迫位置和程度,并急诊行椎管减压术;骨水泥渗漏出现神经根受压表现时,应根据压迫症状的严重程度,决定是否行药物治疗或神经根减压术。对于骨水泥椎旁软组织内、椎间盘内渗漏,一般均不引起特殊临床症状,不需特殊处理,若有软组织酸痛等不适,可予以非甾体类抗炎药对症处理。
当骨水泥椎旁静脉内渗漏时,患者若无特殊不适可不予处理,但应密切观察患者生命体征,并行肺部CT检查,以便早期发现可能的肺栓塞。无症状的肺栓塞仍可予密切观察,不需特殊处理;CT明确肺内存在骨水泥栓子,患者表现为胸痛、呼吸困难时,尽早行抗凝治疗。经治疗后患者症状明显好转或消失,提示抗凝治疗有效,对于症状不缓解者,可在数字减影血管造影下取栓,甚至开胸手术直视下取栓。
5.特殊类型骨折的处理:伴有周壁破损的OVCF行PKP时,骨水泥极易渗漏,尤其是后壁破损的OVCF,骨水泥易渗漏至椎管内压迫脊髓导致瘫痪等严重并发症。因此,周壁破损的OVCF以往常被列为PKP手术的相对禁忌。采用温度梯度灌注技术、骨水泥二次调制灌注封堵技术,并在C臂机动态监测下灌注骨水泥,此类患者可获得安全有效治疗。但术前需常规行CT平扫及三维重建,明确破损部位及大小,做好术前规划。
OVCF骨不愈合的椎体内存在空腔裂隙,裂隙周缘常有瘢痕覆盖,伴骨质硬化,椎体周壁出现较大缺损,行椎体强化手术时骨水泥极易渗漏,且骨水泥不能与周围骨质有效锚合,导致术后骨水泥整块从椎体内脱出。对于此类病例,行骨水泥-骨锚合技术和骨水泥二次调制灌注封堵技术可有效防止骨水泥渗漏,同时使骨水泥在椎体内充分弥散锚合。对于部分伴椎体内巨大空腔的OVCF骨不愈合病例,骨水泥灌注结束前可遗留部分骨水泥拖尾在椎弓根内,以增加锚合面积,防止术后骨水泥松动、移位。
三
术后
(一)术后管理
术后24h佩戴腰围或支具下床适当活动。术后第1天常规进行X线或CT检查。术后应指导患者进行康复训练,如腰背肌功能锻炼等,采用综合治疗方法,积极治疗骨质疏松症。避免大幅度的腰部转体活动和弯腰活动,减少久坐久站,避免坐矮板凳,预防跌倒。
(二)再骨折的预防
PKP术后再骨折包括手术节段再骨折和非手术节段再骨折,而后者又分为邻近椎体再骨折和远隔椎体再骨折。PKP术后再骨折主要发生在邻近椎体。目前,关于PKP术后椎体再骨折究竟是骨质疏松症病程的自然进展,还是PKP手术所致,仍存在较大争议。
预防PKP术后再骨折主要是采取规范的、个体化的、长期的抗骨质疏松治疗方案,从源头上阻止OVCF的发生。首先,采取正确的生活方式,戒烟少酒,多摄入高钙、低盐食物,避免长期使用激素等促进骨量丢失的药物;其次,适度体育活动,多进行户外活动,多接受阳光照射,保持强壮的骨骼;再次,需加强骨质疏松症基础补充剂,如维生素D和钙剂;最后,根据患者个体情况选择合适的抗骨质疏松药物,一般首选一线药物(双膦酸盐类或甲状旁腺素类药物),高骨转换型骨质疏松症患者可选择双膦酸盐类药物,绝经后严重骨质疏松症患者或低骨转换型骨质硫松症患者可选用甲状旁腺素类药物,而对于不适合或不能接受一线药物患者可酌情选用二线药物,如降钙素、维生素K2等。应定期复査骨密度,并根据疗效调整药物。
综上所述,重视PKP的的术前准备、术中操作和术后管理的完整治疗过程的规范化、掌握PKP手术相关的关键技术,学会如何避免和处理PKP应用过程中出现的常见问题,有效降低PKP手术并发症的发生率,精准、安全、有效地实施PKP手术,从而将我国骨质疏松性椎体骨折的诊治水平推上新台阶。
参考文献:略
本文来源:《中华医学杂志》2018年3月20日第98卷第11期













