感染性心内膜炎(IE)是由细菌等病原体感染所致的心内膜,瓣膜或邻近大动脉内膜炎症和伴随的全身性病理过程。按发病情况及病程,可分为急性和亚急性。临床上以亚急性感染性心内膜炎较为常见,多由毒力低的身体某些部位的常在菌所致,起病缓,病程较长。
急性感染性心内膜炎常由毒力强的化脓细菌引起,它们多由身体的其他部位或全身感染侵入心内膜,且病情急,病程短,如不积极治疗,多于数周内死亡。根据感染的部位和是否存在心内植入物,可分为左心自体瓣、左心人工瓣、右心和器械相关性感染性心内膜炎。根据获得的方式,可分为医疗保健相关性、社区获得性和静脉药瘾相关性感染性心内膜炎。
感染性心内膜炎的致病微生物主要为细菌,也可为真菌、病毒、立克次体、衣原体等。急性感染性心内膜炎常见的致病菌为金黄色葡萄球菌、肺炎链球菌、脑膜炎奈瑟菌、流感嗜血杆菌等。亚急性感染性心内膜炎则以甲型溶血性链球菌、肠球菌、表皮葡萄球菌等感染常见。
一、临床表现
1.全身中毒表现
①发热:为本病的最常见症状,除基础状态差的老年人或心肾衰竭的重症患者外,大多数患者在病程中均有不同程度的发热,可伴有全身不适、乏力、纳差、头痛、关节肌肉疼痛、体重减轻等非特异症状。
②进行性贫血:随着病程的延长,贫血呈进行性加重。
③杵状指(趾)、脾大等。
2.心脏杂音
大多数患者可闻及心脏杂音,可以由基础心脏病或心内膜炎导致瓣膜损害所致。急性者比亚急性者更容易出现杂音强度和性质改变,或出现新的杂音。
3.动脉栓塞
可发生脑、肾、脾、肺、肠系膜、视网膜、冠状动脉和肢体动脉栓塞。
4.皮肤、黏膜病损
①瘀点:
由于毛细血管栓塞或毒素使其脆性增加而破裂出血所致。多见于眼结膜、口腔黏膜以及前胸皮肤,中心可发白。
②Osler结节:
为隆起紫红色痛性结节,大小为5~15 mm,多见于手指、足趾端掌面,可能为免疫反应所致。
③Janeway 损害:
位于手掌或足底红色无痛皮损,大小为1~4 mm,多见于急性者,可能为微栓塞所致。
④甲床下条状出血:
远端不到达甲床前边缘,有压痛。
⑤Roth点:
位于眼底或眼结膜中心发白的絮状出血区,多见于亚急性者。
5.并发症
①充血性心力衰竭:
为最常见并发症,主要由瓣膜关闭不全引起。
②细菌性动脉瘤:
多无症状,可扪及搏动性肿块。
③迁移性脓肿:
多发生于肝、脾、骨骼和神经系统。
④神经系统:
除脑栓塞外,可出现脑细菌性动脉瘤、脑出血、脑脓肿、中毒性脑病、化脓性脑膜炎的表现。
⑤肾脏损害:
肾小球肾炎、肾梗死等。
二、诊断要点
血培养是诊断IE的重要方法,血样本应在抗生素治疗开始前在严格无菌操作下采集。2015 年欧洲心脏病学会(ESC) IE 管理指南强调多模态成像技术在IE的诊断中的重要作用。经胸超声心动图(TTE) 可作为疑诊IE患者首选的影像学检查。临床疑似IE,TTE为阳性或非诊断性结果的患者及临床疑诊为IE且植入心脏瓣膜或心脏内装置的患者,推荐再行经食管超声心动图(TOE)检查。
初步检查为阴性,但临床仍高度怀疑E的患者,推荐5~7天内再次行TTE和/或行TOE检查。如怀疑出现新的IE并发症(如新出现心脏杂音、栓塞、持续性发热、心力衰竭、脓肿或房室阻滞)时,应尽早复查TTE和/或TOE。所有需要外科手术的E患者,推荐术中行超声心动图检查。必要时行多层螺旋CT、磁共振、18F -氟脱氧葡萄糖正电子发射断层扫描(PET) /CT 或其他成像技术。
以往IE的诊断标准多采用修订后的Duke诊断标准,2015年ESC指南在此诊断标准基础上补充了3点(见下表):
①心脏CT发现心脏瓣膜周围病变。
②人工瓣膜(植入超过3个月)疑似发生IE,经18F- FDG PET/CT或放射性标记白细胞SPECT/CT发现植入部位附近存在异常活动。
③通过成像技术发现近期发生栓塞事件或感染性动脉瘤。
前两项应视为主要诊断标准,第3项应视为次要诊断标准。
感染性心内膜炎诊断标准

(图源:2015年ESC指南解读)
1. 确诊IE
①2项主要标准;或②1项主要标准加3项次要标准;或③5项次要标准。
2.可能为IE
①1项主要标准加1项次要标准;或②3项次要标准。
三、治疗方案和原则
IE的治疗目的主要是杀灭赘生物中的病原体,防治并发症。
1. 抗生素治疗
①基本原则:应早期、足量、长疗程,静脉使用杀菌剂;
②应根据治疗反应和药敏试验结果及时调整药物种类和剂量;
口腔链球菌和D组链球菌
所致感染性心内膜炎的抗生素治疗方案


葡葡球菌属引起的感染性心内膜炎抗生素治疗方案

肠球菌所致感染性心内腰炎的治疗方案

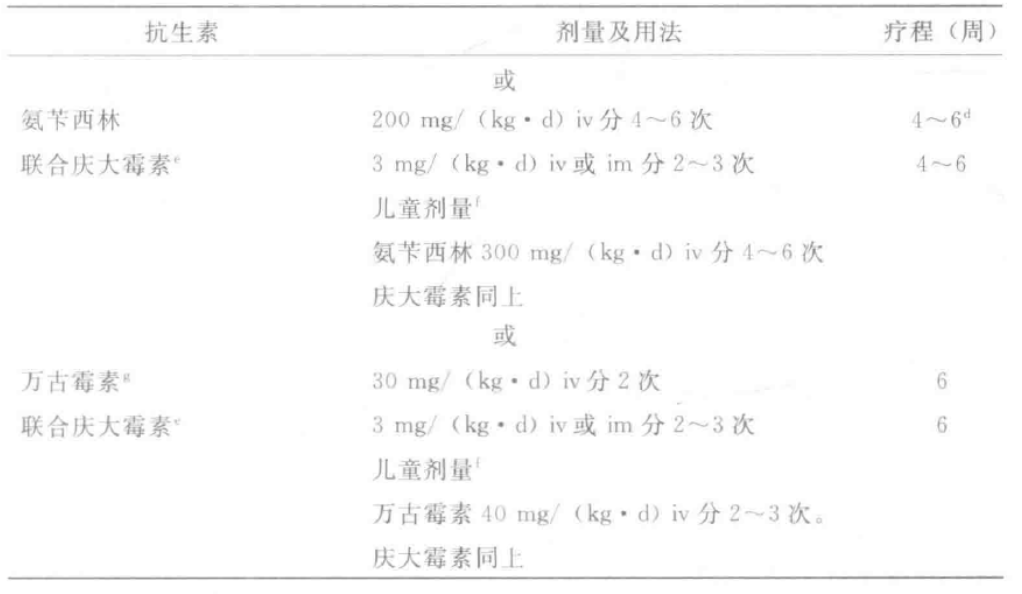
感染性心内膜最初的经验性抗生素治疗方案
(在病原体分离之前或未分离到病原体)
2.外科治疗
一般认为,对于抗生素治愈可能性很小的高危患者和没有严重的合并疾病或并发症但预计单用药物治疗难以康复的患者,应选择外科手术治疗。感染性心内膜炎早期手术的指征主要有心力衰竭,不能控制的感染和防止栓塞事件发生。
参考文献:
[1]陈敏华.超声心动图在感染性心内膜炎患者诊断中的应用价值研究[J].当代医学,2020,26(27):140-141.
[2]Yepez Cristian, Ríos Josias. Pulmonary valve reconstruction using Ozaki's technique for infective endocarditis.. 2020,
[3]宋雨,吴龙,董念国.感染性心内膜炎外科治疗新进展[J/OL].中国胸心血管外科临床杂志:1-10[2020-10-04].http://kns.cnki.net/kcms/detail/51.1492.R.20200908.0958.006.html.
[4]CabreraGarcía Angela I, Müller Franziska, Rödler Frauke S, et al. Infective endocarditis due to Erysipelothrix rhusiopathiae in a dog - a case report.. 2020, 16(1):328-328.
[5]肖秀珍,刘立蓁.3D-TEE与TTE检查对感染性心内膜炎赘生物的诊断效能分析[J].中国医学创新,2020,17(25):128-131.
[6]Luque Paz David, Lakbar Ines, Tattevin Pierre. A review of current treatment strategies for infective endocarditis.. 2020,
[7] Erin McKinnon. A case of tricuspid valve infective endocarditis in intravenous drug use. 2020, 7(3):126-131.
[8]冯增杰.三维经食管心脏超声检查心内膜炎的价值探究[J].中国卫生标准管理,2020,11(16):122-123.
[9] 2015 年欧洲心脏病学会(ESC) IE 管理指南
[10] Sandra Chamat-Hedemand, Anders Dahl, Lauge Østergaard, et al. Prevalence of Infective Endocarditis in Streptococcal Bloodstream Infections Is Dependent on Streptococcal Species. 2020, 142(8):720-730.
[11] Khan Muhammad Zia. Racial and Gender Trends in Infective Endocarditis Related Deaths in United States (2004-2017).. 2020, 129:125-126.
[12] Okada Yukikatsu, Nakai Takeo, Muro Takashi, et al. Mitral valve repair for infective endocarditis: Kobe experience.. 2020, :218492320947586-218492320947586.
本文来源:心希望快讯













