

胰腺癌位列我国男性恶性肿瘤发病率的第7位,女性第11位,占恶性肿瘤相关病死率的第6位。作为预后极差的消化道肿瘤,胰腺癌具有早期诊断困难、手术切除率低、术后易复发转移等临床特点,临床诊治极具挑战性。通过对近年文献的复习总结并结合临床经验对胰腺癌临床诊治的若干热点问题逐一评述并提出推荐意见,以更好地为临床诊治策略及路径选择提供参考和指导胰腺癌的外科治疗。
(1)胰腺癌病人术前营养评估与营养支持
有研究显示,胰腺癌病人合并营养风险及营养不良发生率高达91.1%,高于其他消化系统肿瘤及非胰腺肿瘤病人。我国的多中心回顾性队列研究结果显示,胰十二指肠切除术前营养支持可降低营养风险筛查2002(nutritional risk screening 2002,NRS2002)评分≥5分病人的术后胰瘘发生率。NRS2002是国内外广泛应用的成年住院病人的营养筛查工具,建议至少在术前10 d完成营养筛查,及时发现营养问题以开展必要的营养治疗。NRS2002评分≥3分者即有制定营养诊疗计划的指征,需要进行基本营养评定,包括营养相关病史、膳食调查、体检、实验室检查,在此基础上进行营养干预,包括营养咨询、膳食指导、口服营养补充、肠内营养(管饲)和肠外营养等。
术前营养支持指征:
(1)6个月内体重下降>15%;
(2)BMI<18.5;
(3)主观全面评定法评定为C级;
(4)NRS2002评分>5分;
(5)白蛋白<30 g/L同时肝肾功能正常。
其中指征(1)(2)最常用。对于合并营养风险的多数胰腺癌病人,术前通过膳食指导及口服营养补充(ONS)多可满足营养需求。对存在高营养风险或营养不良的病人,如经口进食不能满足目标量,可进行肠内营养(管饲)、补充性肠外营养或全肠外营养。术前营养支持的时间>7d,强调蛋白质补给量应>1.2g/(kg·d),热量达到生理需求量的70%即可。
推荐意见1:胰腺癌病人术前常规应用NRS2002进行营养风险筛查并制定营养诊疗计划。(证据等级:高;推荐强度:强烈推荐)
推荐意见2:术前营养支持可根据营养状态选择膳食指导、口服营养补充、肠内营养(管饲)和肠外营养等,应用时间至少为7d。(证据等级:中;推荐强度:强烈推荐)
(2)术前胆道引流
采用术前胆道引流(preoperative biliary drainage,PBD)缓解梗阻性黄疸的有效性及必要性存在争议,不建议常规行PBD减黄,因其并不能降低病人围手术期病死率,且可能增加术后并发症发生率。对于胆道梗阻时间较长,肝肾功能明显异常,合并发热及胆管炎等感染表现者,建议行PBD,以控制感染,改善肝肾功能,提高围手术期安全性。如拟行新辅助治疗,治疗前亦应行PBD。是否将黄疸严重程度作为实施PBD的指征,尚无明确结论,多以血清总胆红素≥250 μmol/L(15 mg/dL)作为严重黄疸的定义标准,严重黄疸者术前是否需行PBD,存在争议,建议根据病人实际情况综合判断。提倡内引流减黄,有助于改善病人术前消化及营养状态。
内镜下PBD可选择塑料支架或自膨式金属支架(self-expandable metal stents,SEMS)。有研究认为,SEM易与周围组织发生炎症和粘连,增加了后续手术的难度,塑料支架经济有效且易于取出,但引流期间支架梗阻及移位的发生率明显高于SEMS,较长时间留置时往往需要更换。与塑料支架和未覆膜的SEMS比较,全覆膜SEMS(fully covered SEMS,FCSEMS)通畅时间长,易于移除,更适于新辅助治疗的胰腺癌病人。因此,对于切除可能性大、预计支架留置时间较短的病人可选择塑料支架;对于留置时间可能较长或拟行术前新辅助治疗的病人,可选择FCSEMS。如果无法完成内镜下胆道支架置入,也可选择EUS引导的胆道引流(EUS-BD)。
对于不具备内引流条件如合并上消化道梗阻、狭窄、曾行上消化道重建手术、胆道支架置入失败的病人,可行经皮经肝穿刺胆道引流(percutaneous transhepatic cholangial drainage,PTCD),其对术区影响小,引流效果确切,但胆汁流失不利于病人术前消化及营养状态的改善。
PTCD或内镜支架置入均可能导致相关并发症发生,前者可致出血、胆瘘、感染或腹膜转移等,后者可致急性胰腺炎或胆道感染,建议在较大规模的中心完成上述诊疗行为。
推荐意见3:胰腺癌致胆道梗阻合并胆管炎、计划行新辅助治疗、其他原因导致手术延期等情况时,建议行PBD,且首选内镜下支架置入术。(证据等级:中;推荐强度:一般性推荐)
(3)术前腹腔镜探查在胰腺癌诊治中的应用
胰腺癌姑息性切除无助于改善预后,还可导致全身系统治疗推迟,不利于病人远期生存。此外,胰腺癌术后早期常见肿瘤复发,尤以肝脏、腹膜常见,部分原因是术前即已存在影像学检查难以发现的腹腔或肝脏微小转移。因此,有必要对拟行切除手术且合并高危因素的胰腺癌病人进行全面、仔细的腹腔镜探查,以发现术前影像学未检出的微小转移灶,避免姑息性切除手术。对于无高危因素的可切除胰腺癌病人术前是否常规进行腹腔镜探查,仍有争议,基于腹腔镜探查风险较小而可潜在获益的考虑,可在综合评价后选择性应用。总体评价,胰腺癌局部分期越晚,腹腔镜探查发现远处微转移灶的阳性率越高。
腹腔镜探查应包括腹膜(含小肠及乙状结肠系膜)、肝脏微小转移灶及脱落细胞学检查等。腹腔镜探查证实胰腺癌腹腔微小转移灶的阳性率为11%~56%。研究显示,胰腺癌腹腔脱落细胞学检查阳性率约为10%,尽管脱落细胞学阳性是否等同于远处转移仍有争议,但阳性病人预后更差。
推荐意见4:对于新辅助治疗后的局部进展期及交界可切除胰腺癌病人以及合并高危因素的可切除病人,建议切除手术前行腹腔镜探查。(证据等级:中;推荐强度:强烈推荐)
(4)腹腔镜及机器人手术在胰腺癌外科治疗中的应用
目前腹腔镜及机器人辅助下的各类型胰腺手术均有开展,手术安全性明显提高,技术方面趋于成熟。然而,腹腔镜或机器人辅助手术应用于胰腺癌外科治疗,仍然存在较大争议,主要体现在治疗效果的肿瘤学评价及手术安全性等方面。我国学者进行的前瞻性多中心随机对照研究评价腹腔镜胰十二指肠切除术(laparoscopic pancreatocoduodenectomy,LPD)的安全性,结果显示,对于完成学习曲线、技术成熟的术者,LPD组病人住院时间显著短于开放手术组,两组病人围手术期严重并发症发生率、术后90 d内病死率等差异并无统计学意义。肿瘤学评价方面,有研究显示,LPD淋巴结清扫数目和R0切除率与开放手术比较差异亦无统计学意义,而LPD病人术后住院时间更短,有利于术后早期进行辅助化疗。
有Meta分析显示,LPD术后病人总生存期与开放手术差异无统计学意义,术后肿瘤无复发生存期长于开放手术,故认为微创技术可能为胰腺癌病人带来生存获益。然而,应特别注意学习曲线、术者经验及手术质量对胰腺癌病人围手术期并发症特别是远期预后的影响,微创手术技术应用于胰腺癌的外科治疗,其肿瘤学评价仍有待于高质量的临床研究验证。
推荐意见5:其肿瘤学评价仍有待于高质量的临床研究验证。(证据等级:低;推荐强度:一般性推荐)
(5)根治性顺行模块化胰脾切除术在胰体尾癌治疗中的应用
胰体尾脾切除术是治疗胰体尾癌的标准术式,标准的淋巴结清扫范围须包括脾动脉周围、胰腺下缘及脾门淋巴结,扩大淋巴结清扫范围者还应包括肝总动脉、腹腔干和部分肠系膜上动脉左侧淋巴结。2003年,Strasberg等将根治性顺行模块化胰脾切除术(radical antegrade modular pancreatosplenectomy,RAMPS)应用于胰体尾癌病人,根据是否联合左肾上腺切除分为前RAMPS及后RAMPS,其内涵是对腹膜后切除平面的扩展,强调腹膜后切缘阴性(R0切除)及清扫血管根部淋巴结(图1)。尽管RAMPS对胰腺癌远期预后的改善作用仍存在争议,但因其理论上的合理性及围手术期的安全性,有助于提高胰体尾癌R0切除率,近年来应用日益广泛。
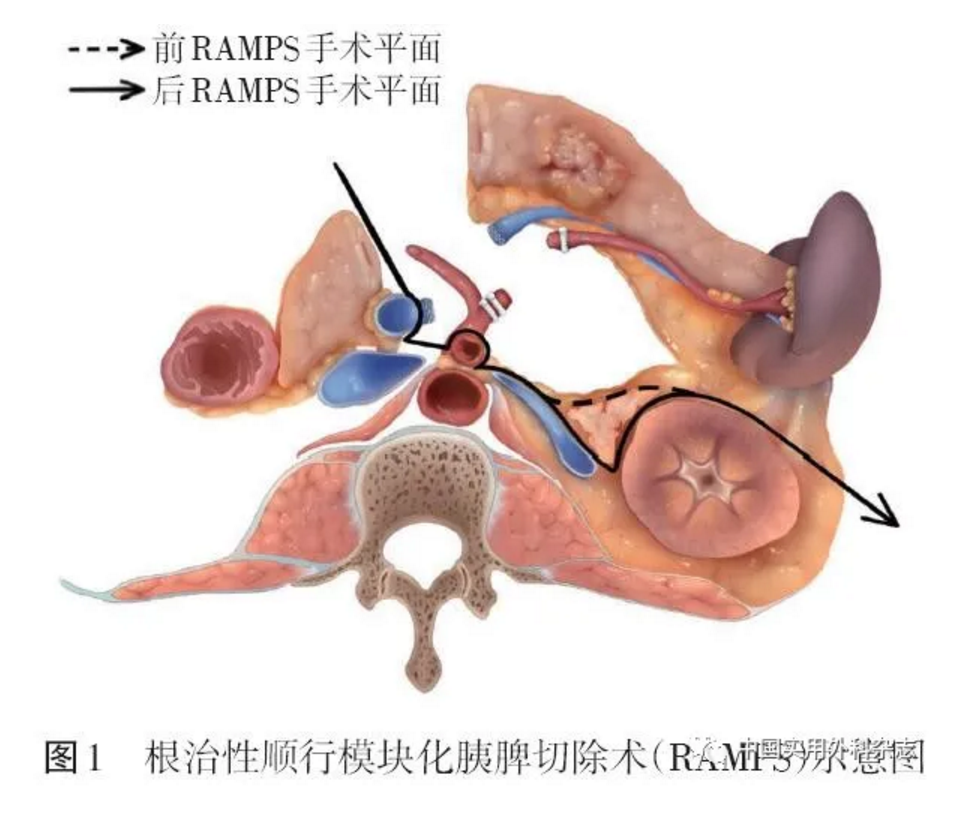
推荐意见6:RAMPS有助于提高胰体尾癌R0切除率,对远期预后的改善作用有待评估。(证据等级:中;推荐强度:一般性推荐)
(6)胰腺癌根治术淋巴结清扫范围
对于胰腺癌相关的淋巴结分组,目前国内外文献及指南多参照日本胰腺协会的命名标准(图2)。
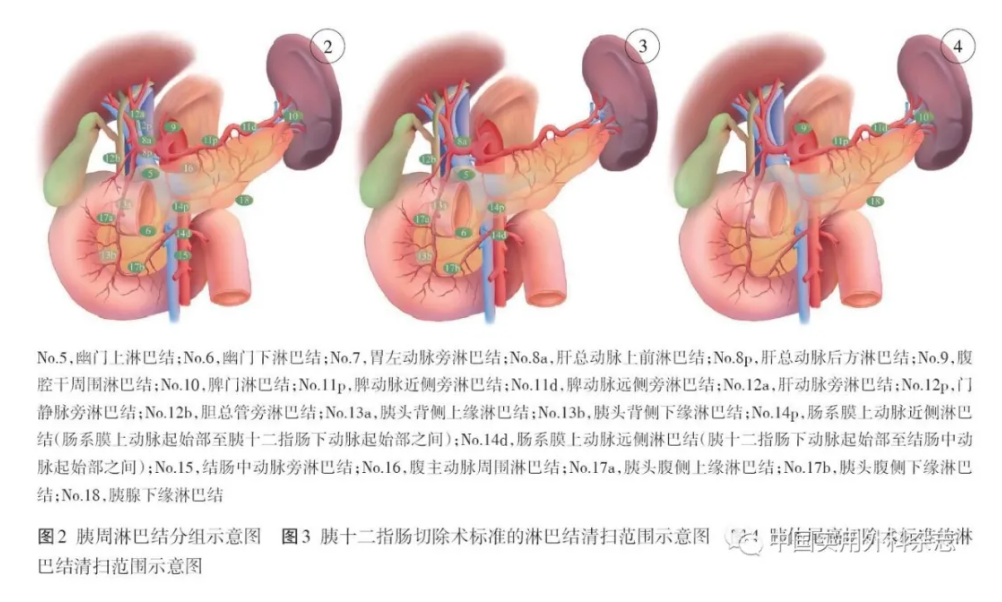
1)胰头癌行胰十二指肠切除术标准的淋巴结清扫范围
标准的淋巴结清扫范围包括:幽门上及下淋巴结(No.5、No.6),肝总动脉前方淋巴结(No.8a),肝十二指肠韧带淋巴结(肝总管、胆总管及胆囊管淋巴结,No.12b),胰十二指肠背侧上缘及下缘淋巴结(No.13a、No.13b),肠系膜上动脉右侧淋巴结(部分No.14),胰十二指肠腹侧上缘及下缘淋巴结(No.17a、No.17b)。完整切除钩突,肠系膜上动脉右侧180°骨骼化。上述淋巴结与标本整块切除。见图3。
不建议常规清扫肝动脉后方(No.8p)及腹主动脉旁(No.16b1)淋巴结,不建议清扫腹腔干(No.9)、胃左动脉(No.7)及脾动脉周围(No.11)淋巴结,不建议全周清扫肠系膜上动脉周围淋巴结(No.14p、No.14d)。
2)胰头癌行胰十二指肠切除术扩大的淋巴结清扫范围
在标准淋巴结清扫范围基础上,清扫肝动脉后方淋巴结(No.8p)、腹腔干周围淋巴结(No.9)、肝固有动脉周围淋巴结(No.12a)、门静脉后方淋巴结(No.12p)、肠系膜上动脉周围淋巴结(No.14p、No.14d)、腹主动脉旁淋巴结(No.16a2、No.16b1)。清扫范围上至肝门,下至肠系膜下动脉起始部,右至右肾门,左至腹主动脉左侧缘,清扫该区域内淋巴结及神经、结缔组织等。
3)胰体尾癌切除术标准的淋巴结清扫范围
脾门淋巴结(No.10)、脾动脉周围淋巴结(No.11)及胰腺下缘淋巴结(No.18)与标本整块切除。对于病灶位于胰体部者,可清扫腹腔干周围淋巴结(No.9)。见图4。对于诊断明确的胰体尾癌病人,应行不保留脾脏的胰体尾切除术。
4)胰体尾癌切除术扩大的淋巴结清扫范围
在标准淋巴结清扫范围基础上,清扫肝总动脉周围淋巴结(No.8)、腹腔干周围淋巴结(No.9)、肠系膜上动脉周围淋巴结(No.14p、No.14d)、腹主动脉旁淋巴结(No.16a2、No.16b1)。
Staerkle等进行的Meta分析中纳入了既往关于淋巴结清扫范围的7项随机对照试验共843例胰腺癌及壶腹周围癌病人的临床资料,结果显示,与标准淋巴结清扫组比较,扩大淋巴结清扫组病人手术时间延长,术中出血量增多,但两组病人围手术期病死率及总生存期差异无统计学意义。Hackert等基于回顾性单臂研究发现,在全身系统治疗模式下,术中清扫以腹腔干、肠系膜上动脉及门静脉为边缘的三角形范围内的神经结缔组织有助于改善局部进展期病人预后,但仍有待高级别证据验证。除临床研究外,目前仍建议行标准淋巴结清扫。
淋巴结清扫数目、阳性淋巴结和总淋巴结数比值与预后的相关性存在争议,但送检标本内一定数量的淋巴结有助于获得准确的N分期,并指导后续辅助治疗。在强调术中淋巴结清扫范围的基础上,提倡外科与病理科联合标准化处理手术标本,应获取15枚以上的淋巴结。
推荐意见7:除临床研究外,胰腺癌术中建议行标准淋巴结清扫,应获取15枚以上淋巴结,以获得准确的淋巴结分期。(证据等级:中;推荐强度:强烈推荐)
(7)联合血管切除的胰腺癌根治术
胰腺癌常累及肠系膜上静脉-门静脉和腹腔干-肝动脉系统,为提高切除率及根治性,常需联合切除受累血管并重建。对于仅肠系膜上静脉-门静脉受累且可切除重建的交界可切除胰腺癌,在全身系统治疗的基础上提倡行联合肠系膜上静脉和(或)门静脉切除的胰十二指肠切除术,如能达到R0切除,病人预后与标准手术组无显著差异,明显优于仅行姑息手术的病人。Meta分析显示,联合静脉切除组病人术中出血量、手术时间、术后住院时间、围手术期并发症发生率及术后30 d内病死率均有显著增加,术后胆瘘、胃排空障碍(DGE)、再手术率和腹腔出血发生率等均高于标准手术组。主要原因在于联合血管切除组病人的肿瘤体积大于对照组,同时合并神经侵犯的比例也明显增加,提示此类病人可能具有更差的生物学行为。
目前,尚无高级别证据支持胰腺癌根治术中联合动脉切除重建。如可行安全的动脉切除重建,且有望获得R0切除,经MDT讨论评估后,可选择手术切除。对于胰体尾癌累及腹腔干者,在全身系统治疗基础上联合腹腔干切除可能改善预后。有回顾性研究显示,新辅助化疗后联合动脉切除的病人中位生存期可达23个月,优于直接手术组病人(13.7个月)。拟行联合动脉切除时,应评估肿瘤侵犯的部位、范围、动脉走行及变异情况,可行数字减影血管造影(DSA)或CT血管成像,结合三维可视化技术,做好术前规划。
由于联合动脉切除的胰腺癌手术的并发症及围手术期病死率均高于未联合动脉切除组,且根治性有限,在手术指征的选择方面应较联合静脉切除持更为审慎的态度。不建议联合肠系膜上动脉切除重建。
推荐意见8:对于有R0切除可能者,提倡行联合肠系膜上静脉和(或)门静脉切除重建的胰腺癌根治术。(证据等级:中;推荐强度:强烈推荐)
推荐意见9:对于动脉受累的胰腺癌病人,应据R0切除可能性、受累部位及是否需要重建等审慎评估手术指征,不建议行联合肠系膜上动脉切除重建。(证据等级:低;推荐强度:一般性推荐。
(8)不可切除胰腺癌的姑息性外科治疗
胰头癌合并消化道梗阻的治疗方式并未达成共识,开放或腹腔镜下胃空肠吻合术以及内镜下消化道支架置入等均为可行之选。内镜下消化道支架置入术具有创伤小、耐受性好、术后恢复快、并发症发生率低、住院时间短等优势,但支架长期留置有移位、闭塞等风险,再干预率较高。外科手术的围手术期并发症发生率高于内镜治疗,但消化道功能恢复更可靠,再干预率较低。对于合并消化道梗阻的晚期胰腺癌病人,预计病人生存期较长(>6个月)且一般情况良好时,建议行胃空肠吻合术,术中可留置肠内营养管路以备术后营养支持;预计生存期较短(<3个月)或一般情况较差无法耐受手术的病人,可行内镜下支架置入。对于尚无消化道梗阻,但在外科手术探查中发现肿瘤无法根治性切除的胰腺癌病人,目前并无证据表明预防性胃空肠吻合术使病人获益,且可能增加围手术期并发症而推迟全身系统治疗时间,故不建议行预防性胃空肠吻合术。
对于合并梗阻性黄疸的不可切除的胰腺癌病人,首选内镜胆道支架置入术。对于支架留置失败或因其他原因无法行内镜治疗的病人,可选择PTCD。姑息性胆肠吻合术仅适于因技术困难或存在禁忌无法通过内镜或PTCD减黄的病人。对于在外科探查术中发现肿瘤无法根治性切除或因消化道梗阻行胃空肠吻合术的病人,若病人已合并胆道梗阻,可行姑息性胆肠吻合术或双旁路手术(胆肠吻合+胃空肠吻合术)。建议切除胆囊,行胆总管-空肠Roux-en-Y吻合。
推荐意见10:对于合并消化道梗阻的晚期胰腺癌病人,根据病人一般状况可选择胃空肠吻合术或内镜下支架置入术。(证据等级:中;推荐强度:强烈推荐)
推荐意见11:对于合并胆道梗阻的不可切除胰腺癌病人,首选内镜支架置入或PTCD。(证据等级:中;推荐强度:强烈推荐)
-----------END--------------
主要文献:
[1] 许静涌,杨剑,陈伟,等. 老年肿瘤住院患者营养不良的横断面调查[J]. 中华老年医学杂志,2019,38(11):1298-1303.
[2] Xu JY,Zhang AR,Tian XD,et al. Preoperative nutrition support based on NRS2002 may reduce the prevalence of postoperative pancreatic fistula (POPF):a retrospective bicenter study of 522 consecutive cases who underwent open pancreatoduodenectomy in China[J]. Pancreas,2019,48(10): 1550.
[3] Lobo DN,Gianotti L,Adiamah A,et al. Perioperative nutrition: Recommendations from the ESPEN expert group[J]. Clin Nutr,2020,39(11):3211-3227.
[4]Gong L,Huang X,Wang L,et al. The effect of preoperative biliary stents on outcomes after pancreaticoduodenectomy: A meta-analysis[J]. Medicine (Baltimore),2020,99(42):e22714.
[5] Crippa S,Cirocchi R,Partelli S,et al. Systematic review and meta-analysis of metal versus plastic stents for preoperative biliary drainage in resectable periampullary or pancreatic head tumors[J]. Eur J Surg Oncol,2016,42(9):1278-1285.
[6] Allen VB,Gurusamy KS,Takwoingi Y,et al. Diagnostic accuracy of laparoscopy following computed tomography (CT) scanning for assessing the resectability with curative intent in pancreatic and periampullary cancer[J]. Cochrane Database Syst Rev,2016,7(7):CD009323.
[7] Cao F,Li J,Li A,et al. Prognostic significance of positive peritoneal cytology in resectable pancreatic cancer: a systemic review and meta-analysis[J]. Oncotarget,2017,8(9):15004-15013.
[8] Wang M,Li D,Chen R,et al. Laparoscopic versus open pancreatoduodenectomy for pancreatic or periampullary tumours:A multicentre,open-label,randomised controlled trial[J]. Lancet Gastroenterol Hepatol,2021,6(6):438-447.
[9] Palanivelu C,Senthilnathan P,Sabnis SC,et al. Randomized clinical trial of laparoscopic versus open pancreatoduodenectomy for periampullary tumours[J]. Br J Surg,2017,104(11):1443-1450.
[10] Poves I,Burdío F,Morató O,et al. Comparison of perioperative outcomes between laparoscopic and open approach for pancreatoduodenectomy: The PADULAP randomized controlled trial[J]. Ann Surg,2018,268(5):731-739.
[11] van Hilst J,de Rooij T,Bosscha K,et al. Laparoscopic versus open pancreatoduodenectomy for pancreatic or periampullary tumours (LEOPARD-2): A multicentre,patient-blinded,randomised controlled phase 2/3 trial[J]. Lancet Gastroenterol Hepatol,2019,4(3):199-207.
[12]Peng L,Zhou Z,Cao Z,et al. Long-term oncological outcomes in laparoscopic versus open pancreaticoduodenectomy for pancreatic cancer: A systematic review and Meta-analysis[J]. J Laparoendosc Adv Surg Tech A,2019,29(6):759-769.
[13] Strasberg SM,Drebin JA,Linehan D. Radical antegrade modular pancreatosplenectomy[J]. Surgery,2003,133(5):521-527.
[14]Cao F,Li J,Li A,et al. Radical antegrade modular pancreatosplenectomy versus standard procedure in the treatment of left-sided pancreatic cancer: A systemic review and meta-analysis[J]. BMC Surg,2017,17(1):67.
[15] 陈凯,王琦,高红桥,等. 根治性顺行模块化胰脾切除术治疗胰体尾癌安全性与有效性的Meta分析[J]. 腹腔镜外科杂志,2019,24(9):665-671.
[16 ] Staerkle RF,Vuille-Dit-Bille RN,Soll C,et al.Extended lymph node resection versus standard resection for pancreatic and periampullary adenocarcinoma[J]. Cochrane Database Syst Rev,2021,1:CD011490.
[17] Hackert T,Strobel O,Michalski CW,et al. The TRIANGLE operation - radical surgery after neoadjuvant treatment for advanced pancreatic cancer: a single arm observational study[J]. HPB (Oxford),2017,19(11):1001-1007.
[18]Peng C,Zhou D,Meng L,et al. The value of combined vein resection in pancreaticoduodenectomy for pancreatic head carcinoma: a meta-analysis[J]. BMC Surg,2019,19(1):84.
[19] Bachellier P,Addeo P,Faitot F,et al. Pancreatectomy with arterial resection for pancreatic adenocarcinoma: How can it be done safely and with which outcomes?A single institution's experience with 118 patients[J]. Ann Surg,2020,271(5):932-940.
[20] Martin-Perez E,Domínguez-Muñoz JE,Botella-Romero F,et al. Multidisciplinary consensus statement on the clinical management of patients with pancreatic cancer[J]. Clin Transl Oncol,2020,22(11):1963-1975.
声明:来源于中华外科杂志,如有侵权请联系删除。













