引用格式:中华医学会运动医疗分会, 中国医师协会骨科医师分会运动医学学组, 中国医师协会骨科医师分会关节镜学组. 骨关节炎临床药物治疗专家共识[J]. 中国医学前沿杂志(电子版), 2021, 13(7): 32-43.
骨关节炎临床药物治疗专家共识
中华医学会运动医疗分会,中国医师协会骨科医师分会运动医学学组,中国医师协会骨科医师分会关节镜学组
通信作者 :
陈世益 E-mail :cshiyi@163.com ;
王坤正 E-mail :yangpei@vip.163.com ;
李 箭 E-mail :lijianchina@163.com
01
背 景
骨关节炎(osteoarthritis,OA)是由多种因素引起的以关节软骨磨损、皲裂、溃疡、脱失,关节软骨下骨及周围骨反应、滑膜炎性反应、关节周围肌肉萎缩,关节疼痛、关节功能下降的退行性关节病,易发生于中老年人群,发病率高,65岁以上膝痛人群有超过50%为OA患者,75岁以上膝痛人群中的OA患病率超过80%[1,2]。OA病因尚不完全明确,其发生与年龄、肥胖、炎症、创伤及遗传因素等有关。
OA的病理特点为关节软骨变性破坏、软骨下骨硬化或囊性变、关节边缘骨质增生、滑膜病变、关节囊挛缩、韧带松弛或挛缩、肌肉萎缩无力等[3]。
OA的临床表现为,①关节疼痛:关节疼痛是OA最常见的临床表现,以膝、指间及髋关节最常见[4,5]。初期为轻度或中度间断性隐痛,休息后好转,活动后加重;晚期可出现持续性疼痛或夜间痛。②关节活动受限:常见于膝、髋关节,晨起时关节僵硬及发紧感(俗称晨僵)活动后可缓解,但晨僵持续时间极少超过30 min[6]。③关节畸形:由软骨破坏、骨性增生、骨赘形成、滑膜炎所致[7],以指间关节OA最常见。④骨摩擦音(感):常见于膝关节OA[6],因关节软骨破坏,关节面不平整所致。⑤肌肉萎缩:常见于膝关节OA,因关节疼痛和活动减少及退化所致。
X线检查已成为OA影像学诊断的重要依据,是首选的影像学检查。在X线片上OA的三大典型表现为:受累关节非对称性关节间隙变窄,软骨下骨硬化和/或囊性变,关节边缘骨赘形成。部分患者关节内可见游离体,甚至下肢力线改变。MRI和CT对于临床诊断早期OA有一定价值,目前多用于OA的鉴别诊断或临床研究[8]。
OA的诊断标准需根据患者病史、症状、体征、X线表现及实验室检查作出临床诊断和鉴别诊断。关于膝关节、髋关节、指间关节OA诊断标准可参照2018年中华医学会骨科学分会关节外科学组制定的《骨关节炎诊疗指南(2018年版)》[6],OA X线的Kellgren & Lawrence分级(K-L分级)见表1[6]。

OA需积极干预,治疗目的是缓解疼痛,延缓疾病进展,矫正畸形,改善或恢复关节功能,提高患者生活质量。
OA的治疗遵循阶梯化、个体化系统治疗原则,①基础治疗:有/无症状的OA患者均需干预,接受健康教育,改变不良生活和工作方式,采用个体化运动处方方案,增加关节活动度和周围肌肉力量维护锻炼,保护性使用关节,物理治疗等,预防OA进行性加重;②症状较轻者适当休息,避免受凉,需对患者进行康复指导和运动处方指导;③症状明显者除康复指导外,还需药物治疗,急性期患者需注意休息;④对有外科手术适应证和重度OA患者(非手术治疗无效)可以采用手术治疗,包括关节镜下清理术、软骨修复术、截骨矫形术、关节融合术、关节重建术等。
OA患者的健康教育:①自我调控,避免和减少不利因素,如控制好体重、劳逸结合;②避免创伤和不良姿势;③注意保暖,防止受凉受潮,使用护膝、护腰、软底鞋;④使用辅助装置,防止关节过度使用,与职业有关者应调换工种;⑤以运动处方指导合理锻炼等。
近3年关于OA的指南和专家共识有很多,包括2018年中华医学会骨科学分会关节外科学组制定的《骨关节炎诊疗指南(2018年版)》,2018年中华医学会骨科学分会关节外科学组联合吴阶平医学基金会骨科学专家委员会制定的《膝骨关节炎阶梯治疗专家共识(2018年版)》,2020年中华医学会骨科学分会关节外科学组制定的《中国骨关节炎疼痛管理临床实践指南(2020年版)》等,均提出了OA金字塔型的阶梯化分级治疗策略,即基础治疗、药物治疗、修复性治疗和重建治疗。其中,基础治疗和药物治疗贯穿OA治疗的全程。但是,不治疗、非甾体抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs)和糖皮质激素类药物等的不合理用药现象在OA的治疗中并不少见,同时存在过度治疗、药物滥用的现象。基于此,中华医学会运动医疗分会、中国医师协会骨科医师分会运动医学学组、中国医师协会骨科医师分会关节镜学组组织专家编写了《骨关节炎临床药物治疗专家共识》,旨在进一步指导临床安全、有效、经济和规范地使用OA治疗药物,为OA患者整体关节健康提供保障。
02
骨关节炎药物治疗的重要性
药物治疗在OA的整体治疗中占有重要地位,大多数患者都需要短期或长期药物治疗,贯穿于有症状患者的全治疗过程。药物治疗具有简便易行、疗效可靠及依从性好等优点。
目前OA的药物治疗已逐渐从较单一的抗炎、镇痛、缓解症状转向多方位的改善病情治疗。根据患者的病变部位和病变程度不同,采取早期、联合、长程、个体化的治疗策略是目前OA药物治疗的有效方式。医生必须充分了解药物的作用机制、适应证和不良反应,同时考虑患者的关节症状和合并症,做到合理用药,避免不合理用药造成的不良反应,减少损害。如合并其他疾病,需要配合使用具有不同作用机制的药物,使各种药物相互兼容,协同发挥作用。
然而在OA治疗过程中不正确和不合理用药的现象仍然存在,这不仅延误疾病治疗,浪费医药资源,还可能导致药源性疾病,甚至医疗不良事件的发生。迄今为止,并没有专门针对OA合理用药的相关共识。因此,指导OA患者合理用药,是临床亟待解决的问题之一。
03
骨关节炎治疗药物的种类与特性
OA治疗药物有多种分类方法,为方便临床使用,根据用药方式分为以下7类:局部外用药、口服药、肛门栓剂、肌内注射药、静脉注射药、关节腔内注射药及其他(如生物制剂等)。
3.1 局部外用药
由于外用药物作用于局部,经皮肤渗透发挥作用,具有局部浓度高、系统暴露量少、全身不良反应少等优势,成为药物治疗的优选。根据不同作用机制、剂型、不良反应进行合理选用非常重要。
3.1.1 适应证
轻度OA患者、高龄或合并基础疾病较多的患者或对口服药有胃肠道反应的患者,建议优先选择局部外用药。中、重度OA患者可联合口服NSAIDs。
3.1.2 禁忌证
当皮肤有伤口、皮疹及局部有感染等不良状况时应禁用,出现过敏反应时及时停药。
3.1.3 分类
3.1.3.1 外用NSAIDs
其作用机制见3.2.1.1。在所有外用镇痛药中,外用NSAIDs的疗效最显著[9]。目前已上市的药物包括双氯芬酸、洛索洛芬、酮洛芬、布洛芬等,剂型也有所不同,如贴剂、凝胶剂、乳剂/膏、溶液剂、喷雾剂等。常见治疗OA的外用NSAIDs包括双氯芬酸二乙胺乳胶剂、洛索洛芬钠贴剂、布洛芬凝胶、酮洛芬凝胶、氟比洛芬凝胶贴膏等。外用NSAIDs的凝胶制剂较易被局部组织吸收,疗效更佳。局部使用洛索洛芬钠贴剂治疗膝关节OA的效果不劣于洛索洛芬钠片剂[10];凝胶制剂等较易被局部组织吸收,疗效更直接,研究显示酮洛芬凝胶较普通剂型疗效明显提升。治疗OA的常见外用NSAIDs用法和用量见附表1。
3.1.3.2 非NSAIDs擦剂
主要通过影响神经肽P物质的释放和储存而发挥镇痛和止痒作用,用于缓解关节或肌肉疼痛,如外用辣椒碱等。
3.1.3.3 中药膏剂
将中药方剂制成贴膏、膏药和药膏。其功效以补益肝肾、活血通络、强筋健骨、改善骨代谢、缓解疼痛为主。
3.1.3.4 外用麻醉剂
常用药物如芬太尼透皮贴剂等。
(1)适应证:治疗中、重度慢性疼痛以及仅能依靠阿片样镇痛药治疗的难以消除的疼痛。
(2)禁忌证:对贴剂中黏附剂敏感的患者。
3.1.4 用药建议
正确选择和使用局部外用药,涂、擦、贴应时间充足,均匀,间隔和用药量到位。
3.1.5 不良反应
贴剂应避免张力过高而引起张力性水疱,对于发痒和已发生皮疹反应的患者应及时停用,并清理皮肤,行抗过敏治疗。
3.2 口服药
根据药物作用机制和目的分为减轻症状、改善功能类,延缓病情进展类,抗骨质疏松症类,抗焦虑类,中成药等。
3.2.1 减轻症状、改善功能类
3.2.1.1 NSAIDs
口服NSAIDs是目前控制OA相关症状的首选药物。
(1)作用机制:抗炎、解热、镇痛、缓解局部骨赘刺激引起的炎症症状,减轻关节肿胀等。
(2)适应证:用于症状性OA。口服药物由胃肠道吸收,可以达到较高的血药浓度,同时不良反应也相对较多。
(3)禁忌证:活动性消化道溃疡和近期胃肠道出血者,对阿司匹林或其他NSAIDs过敏者,肝功能不全者,肾功能不全者,严重高血压和充血性心力衰竭患者,血细胞减少者,妊娠期和哺乳期女性。
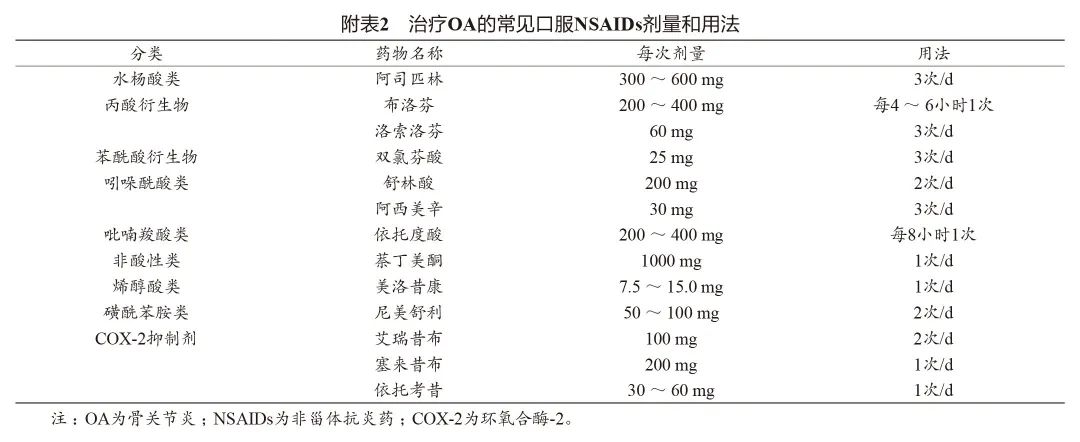
(4)分类:环氧合酶(cyclooxygenase,COX)是NSAIDs的主要作用靶点,根据对COX的选择性,分为非选择性COX抑制剂和选择性COX-2抑制剂。目前国内治疗OA的常用口服NSAIDs包括阿司匹林、布洛芬、洛索洛芬、双氯芬酸、舒林酸、阿西美辛、依托度酸、萘丁美酮、美洛昔康、尼美舒利、艾瑞昔布、塞来昔布、依托考昔等。治疗OA的常见口服NSAIDs剂量和用法见附表2。
(5)用药建议:①宜选用对软骨基质蛋白聚糖合成有促进作用的NSAIDs,如洛索洛芬、艾瑞昔布、塞来昔布、双氯芬酸、美洛昔康、醋氯芬酸等。②在1种NSAIDs足量使用1~2周无效后再更改为另1种;避免同时服用≥2种NSAIDs。③不要空腹服药,用药期间不建议饮酒;不宜与抗凝药(如华法林)联用,可能增加出血风险。④必要时可选择特殊剂型,如肠溶剂型可减少对胃黏膜的刺激,而缓释剂型能较好地控制血药浓度,提高患者对药物的依从性。
(6)不良反应:①胃肠道,恶心、呕吐、腹痛、腹泻、腹胀、食欲不佳,严重者有消化道溃疡、出血、穿孔等;推荐使用质子泵抑制剂(proton pump inhibitor,PPI),如奥美拉唑、兰索拉唑、泮托拉唑等。②肾脏,肾灌注量减少,出现水钠潴留、高血钾、血尿、蛋白尿、间质性肾炎,严重者发生肾坏死致肾功能不全。③血液系统,外周血细胞减少、凝血功能障碍、再生障碍性贫血。④少数患者发生过敏反应(皮疹、哮喘)、肝功能损害、耳鸣、听力下降和无菌性脑膜炎等。
3.2.1.2 对乙酰氨基酚
(1)作用机制:通过抑制前列腺素E1(prostaglandin E1,PGE1)、缓激肽和组胺等的合成和释放,提高痛阈而发挥镇痛作用,属于外周性镇痛药,作用弱于阿司匹林。
(2)适应证:仅对轻、中度OA所致疼痛有效,对胃肠黏膜、肝、肾较安全。
(3)禁忌证:对本品过敏和严重肝肾功能不全者禁用。
(4)用药建议:OA伴轻、中度疼痛患者通常选用对乙酰氨基酚,每日最大剂量不超过2 g,如有肝肾疾病、摄入危险剂量酒精、老年人,剂量应减半;对乙酰氨基酚治疗效果不佳的OA患者,可个体化使用NSAIDs。
(5)不良反应:偶见皮疹、荨麻疹、药物热及粒细胞减少。长期大量用药会导致肝肾功能异常。
3.2.1.3 阿片类药物
(1)作用机制:阿片类药物的镇痛作用机制是多平面的,外周神经有阿片受体;阿片类药物可与位于脊髓背角胶状质(第二层)感觉神经元上的阿片受体结合,抑制P物质的释放,从而阻止疼痛传入脑内;阿片类药物也可作用于大脑和脑干的疼痛中枢,发挥下行疼痛抑制作用。
(2)适应证:适用于对NSAIDs有禁忌或无效者,但由于其不良反应和成瘾性发生率相对较高,2019年国际骨关节炎研究协会发布的骨关节炎指南中强烈反对在OA疼痛管理中应用口服或外用阿片类药物[11];《中国骨关节炎疼痛管理临床实践指南(2020年版)》也不推荐将阿片类药物(含曲马多)作为缓解OA患者疼痛的一线药物[12]。
(3)禁忌证:支气管哮喘,上呼吸道梗阻,严重肝肾功能障碍,伴颅内高压的颅内占位性病变,未明确诊断的急腹症,妊娠期、待产期和哺乳期女性,1岁以内婴儿。
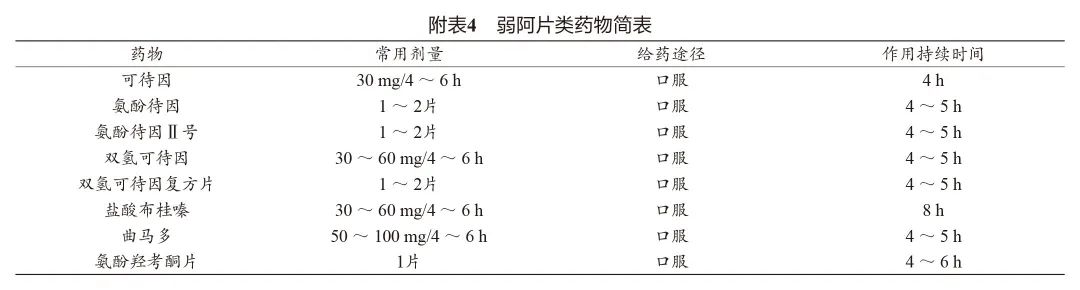
(4)分类:常见阿片类药物如硫酸(盐酸)吗啡控释片、盐酸羟考酮控释片、可待因、氨酚待因、双氢可待因、盐酸布桂嗪、曲马多、氨酚羟考酮片等。强阿片类药物简表见附表3,弱阿片类药物简表见附表4。
(5)用药建议:用药前需进行风险评估,关注潜在内科疾病风险。根据患者个体情况,剂量个体化,且尽量使用最低有效剂量,避免过量用药、同类药物重复或叠加使用。用药3个月,根据病情选择检查血常规、大便常规、大便潜血及肝肾功能。
(6)不良反应:呼吸抑制、心悸、恶心、依赖性等。
3.2.2 延缓病情进展类
3.2.2.1 双醋瑞因
双醋瑞因是在桂皮属植物中发现的具有天然抗炎属性的蒽醌类衍生药物,具有抗炎、保护关节软骨的作用。
(1)作用机制:双醋瑞因是白介素-1(interleukin-1,IL-1)抑制剂,通过抑制IL-1的产生和活性以及后续的作用,抑制软骨降解、促进软骨合成并抑制滑膜炎症,能有效改善OA的症状,减轻疼痛,改善关节功能,还可延缓OA病程进展。
(2)适应证:对于OA慢性疼痛的患者可用于镇痛[12]。
(3)禁忌证:对双醋瑞因过敏或有蒽醌衍生物过敏史的患者以及既往有肠道不适(尤其是过敏性结肠炎)的患者禁用。
(4)用药建议:由于双醋瑞因于治疗后2~4周显效,且具有良好的胃肠道耐受性,建议在给药的最初2~4周可与其他镇痛药或NSAIDs联用,总疗程不应短于3个月。
3.2.2.2 氨基葡萄糖
(1)作用机制:提供蛋白聚糖合成的物质,补充内源性软骨成分;刺激软骨细胞产生有正常多聚体结构的蛋白多糖,促进滑膜合成透明质酸;抑制损伤软骨的酶,如基质金属蛋白酶、胶原酶、磷脂酶A2等;抑制超氧化物自由基的产生。
(2)适应证:轻度OA。对关节软骨严重磨损的终末期OA疗效不佳。有研究认为该类药物有缓解疼痛症状、改善关节功能、延缓病情进展的作用,但也有研究认为其并不能延缓疾病进展[13,14]。目前,该类药物对OA的临床疗效尚存争议[15],对有症状的OA患者可选择性使用。欧洲骨质疏松、骨关节炎及肌肉骨骼疾病临床与经济学会(the European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases,ESCEO)推荐将结晶型硫酸氨基葡萄糖作为膝关节OA的长期基础治疗药物。
(3)禁忌证:对本品过敏者禁用。
(4)用药建议:分为硫酸氨基葡萄糖和盐酸氨基葡萄糖,相较而言,硫酸氨基葡萄糖胃肠道刺激更小,更易吸收。大多数研究结果提示持续应用1500 mg氨基葡萄糖8周以上才能显示一定的疗效。推荐餐时或餐后服用,可减轻胃肠道不适,特别是有胃溃疡的患者。
3.2.3 抗骨质疏松症类
已有研究表明,OA与骨质疏松症具有明显的相关性,但同时也存在争议[16]。有些药物可同时治疗OA和骨质疏松症这两种疾病。
3.2.4 抗焦虑类
可应用于长期持续疼痛的OA患者,尤其是对NSAIDs不敏感的患者[17],可改善患者的抑郁和焦虑等精神改变,还可增加中枢神经的下行性疼痛抑制系统功能。其不良反应包括胃肠道反应、口干等[18]。目前,其治疗OA的远期效果尚需随访,用药类型和剂量建议在专科医生指导下使用。
3.2.5 中成药
可通过多种途径发挥减轻疼痛、延缓OA疾病进程、改善关节功能的作用。
3.3 肛门栓剂
具有吸收快、起效快的特点。
3.3.1 适应证
不便口服药物的患者。
3.3.2 禁忌证
有活动性消化道溃疡/出血或重度心力衰竭患者禁用,老年患者易发生不良反应,应慎用或调整使用剂量。
3.3.3 分类
常用的是NSAIDs(如吲哚美辛栓)。
3.4 肌内注射药
3.4.1 适应证
不宜或不能静脉注射及其他治疗无效的患者,要求较皮下注射更迅速产生疗效及注射刺激性较强或药量较大的药物时。
3.4.2 分类
常用的药物有阿片类药物(盐酸布桂嗪、曲马多)等。治疗OA的常见阿片类肌内注射药物用法和用量见附表5。
3.5 静脉注射药
需在医疗机构内使用。
3.5.1 适应证
不便口服药物及其他方式药物治疗无效的患者。
3.5.2 特点
具有起效快、调整剂量方便的优点,但作用强且难于逆转,可能会为患者带来较大风险,应遵循能口服就不要静脉输注的原则。
3.5.3 分类
常用的药物有NSAIDs(如帕瑞昔布钠)、氟比洛芬酯、阿片类药物等。治疗OA的常见静脉注射NSAIDs用法和用量见附表6。
3.6 关节腔内注射药
可有效缓解疼痛,改善关节功能。但该方法是侵入性治疗,可能会增加感染的风险,必须严格无菌操作和规范操作。
常用的药物有糖皮质激素、医用几丁糖、玻璃酸钠等。
共同禁忌证:①感染性关节炎;②注射部位附近或有全身感染者;③凝血功能异常者;④对相关药物过敏的患者;⑤其他不适宜关节腔注射的情况。
3.6.1 糖皮质激素
起效迅速,短期缓解疼痛效果显著[19]。
3.6.1.1 作用机制
可降低毛细血管的通透性,减轻炎性反应造成的充血、组织液渗出及炎性细胞浸润[20,21]。可抑制IL-1、白介素-6(interleukin,IL-6)、干扰素(interferon,IFN)和肿瘤坏死因子(tumor necrosis factor,TNF)等炎性因子的释放,降低血管内皮细胞对白细胞的黏附性;可抑制磷脂酶A2的活性,继而减少前列腺素E2(prostaglandin E2,PGE2)、白三烯和血小板活化因子(platelet activating factor,PAF)的合成与释放,进而终止炎症进程[22]。
3.6.1.2 适应证
可改善轻度OA早期肿痛症状,但对重度OA的严重疼痛,其作用甚微[23]。
3.6.1.3 禁忌证
对激素过敏者,局部或全身细菌、病毒和真菌等各种感染,曾患或现患严重精神疾病,活动性消化性溃疡病,新近行胃肠吻合手术,严重高血压、糖尿病等。
3.6.1.4 用药建议
建议同一关节每年应用最多不超过2~3次,注射间隔时间不应短于3~6个月[26,27]。
3.6.1.5 不良反应
反复多次应用激素会对关节软骨产生不良影响[24],与其抑制软骨细胞的增殖和促进凋亡、影响软骨内基质的新陈代谢[25]、破坏软骨下骨的生理环境有关。
3.6.2 医用几丁糖
3.6.2.1 作用机制
体外实验显示,几丁糖或经修饰过的几丁糖可以促进软骨细胞外基质的合成,减轻炎性反应,调节软骨细胞代谢[28]。其具有的黏弹性特征类似于透明质酸,可以作为关节液的补充成分,减缓关节炎的进展[28,29]。
3.6.2.2 适应证
适用于轻、中度OA患者。
3.6.2.3 禁忌证
严重的关节畸形,损伤严重的创伤性关节炎,急慢性出血性关节炎症。
3.6.2.4 用药建议
每个疗程注射2~3次,每年1~2个疗程。
3.6.2.5 不良反应
过敏反应,局部发热和红肿。
3.6.3 玻璃酸钠
3.6.3.1 作用机制
保护软骨细胞;促进蛋白聚糖和糖胺聚糖合成;抗炎;机械润滑;保护软骨下骨;镇痛;促进内源性玻璃酸钠分泌;保护半月板[30]。
3.6.3.2 适应证
可用于治疗膝、肩、踝、髋、肘、腕等关节的OA,对轻、中度OA患者效果更显著[31,32]。玻璃酸钠可减少NSAIDs等口服镇痛药的用量,特别适用于老年人、既往有消化道溃疡病史、出血史、心脑血管疾病病史的患者,可减少其他药物导致的胃肠道不良反应和心血管不良事件。
3.6.3.3 禁忌证
关节内或穿刺局部有感染者;对禽类或蛋类过敏者应慎用;其他原因引起的关节肿胀和积液。
3.6.3.4 用药建议
每次注射剂量为1支,每周注射1次;根据药物不同,3~5周为1个疗程,每年1~2个疗程。
3.6.3.5 不良反应
注射局部轻或中度疼痛、肿胀或关节积液,多可自行缓解。
3.7 生物制剂
3.7.1 富血小板血浆
3.7.1.1 作用机制
富血小板血浆(platelet rich plasma,PRP)富含多种生长因子和炎症调节因子,具有保护软骨细胞、促进软骨愈合和减轻关节内炎症的作用[33-35]。但目前其作用机制和长期疗效尚需进一步研究[36]。
3.7.1.2 适应证
对年轻[37]、X线轻/中度或MRI有退行性表现的症状性OA患者更适用[38]。
3.7.1.3 禁忌证
注射区周围有皮肤病或皮肤破溃,不能除外其他疾病引起的关节明显肿胀、积液,凝血功能异常者,败血症。
3.7.1.4 用药建议
每次注射剂量以3~5 ml较多见。间隔时间一般为1~3周,2~3次为1个疗程。
3.7.1.5 不良反应
关节内感染,注射区局部疼痛或红肿。
3.7.2 IL-1受体拮抗剂
IL-1是介导OA中关节软骨破坏最重要的细胞因子。目前已证实IL-1受体拮抗剂有逆转OA关节软骨结构和生化性能的潜力,但其对OA的预防、早期诊断及治疗仍处于探索阶段[39]。
3.7.3 抗炎性细胞因子
可减少IL-1β和TNF-α的生成。细胞因子信号通路的抑制剂等生物制剂的探索为未来靶向治疗OA提供了新的方向[40]。
3.7.4 间充质干细胞
间充质干细胞广泛存在于各类组织中,经诱导后可分化为成骨细胞或软骨细胞,可用于修复受损的骨或软骨,在OA的治疗中已有应用,但其临床疗效和安全性尚需大量随机对照试验验证[41]。
04
骨关节炎用药的合理性和基本原则
OA药物治疗的目的是减轻或消除疼痛等症状,改善关节功能,延缓病情进展,提高患者生活质量,多以口服NSAIDs和延缓病情进展类药物为主要治疗方式。因此,根据OA患者病变部位、分期,尤其是疼痛程度,进行内外结合、个体化、阶梯化合理药物治疗十分必要。
4.1 不同分期和不同病变选用药物的合理性
4.1.1 无症状或偶有轻微症状
患者偶发关节疼痛,可正常进行日常活动,无关节肿胀,无明显畸形。X线片显示关节间隙可疑狭窄,轻微骨赘,K-L分级Ⅰ级。对于此类患者,以基础治疗为主,主要包括健康教育、功能锻炼、物理治疗、行为支持治疗及运动治疗。对基础治疗不佳者,可局部外用NSAIDs类凝胶剂、贴剂或中药提取物乳膏,如双氯芬酸、酮洛芬、布洛芬、洛索洛芬、氟比洛芬、辣椒碱等。不建议采用全身镇痛药物治疗。局部用药镇痛效果不佳时,需经临床医生严格评估风险后,换用口服镇痛药或联合用药。
4.1.2 轻度
患者经常出现关节疼痛,基本不影响日常活动,浅表关节偶发肿胀,无明显畸形。X线片显示关节间隙轻度狭窄,有小骨赘,K-L分级Ⅱ级。对于此类患者,应以药物治疗为主,结合基础治疗。口服NSAIDs存在不良反应发生风险,多用于对乙酰氨基酚治疗无效的患者[15,42-45]。NSAIDs用药原则包括使用最小有效剂量、尽可能缩短持续用药时间、尽量局部用药,严重疼痛时口服和局部联合用药[26,46-48]。老年患者宜选用半衰期短的NSAIDs,如双氯芬酸、吲哚美辛、洛索洛芬钠片等;既往有消化道溃疡病史的患者,宜服用选择性COX-2抑制剂;联合胃肠道黏膜保护剂,可减少胃肠道不良反应。需警惕心肌梗死等发生风险。联用延缓病情进展类药物和软骨保护剂,包括双醋瑞因、氨基葡萄糖、葡糖胺聚糖等。长期使用双醋瑞因治疗,每日1~2次,每次1粒,餐后服用,不短于3个月。轻度OA患者持续应用1500 mg氨基葡萄糖8周以上,而使用1年以上疗效更稳定。关节腔注射药物包括玻璃酸钠、医用几丁糖等,可有效缓解疼痛,改善关节功能。不建议口服阿片类药物以及关节腔内注射糖皮质激素。
4.1.3 中度
患者疼痛经常出现,日常活动受限,浅表关节经常肿胀,可出现畸形。X线片提示关节间隙狭窄明确,有中等量骨赘形成,可出现关节畸形,K-L分级Ⅲ级。口服NSAIDs是首选治疗方案,需要长期服药。优先考虑选择性COX-2抑制剂或同时服用PPI类药物以减轻胃肠道不良反应。建议联合延缓病情进展类药物和软骨保护剂。合并关节软骨破坏、半月板撕裂、机械交锁等,建议在关节软骨修复术或关节镜检清理术的基础上,于关节腔内注射玻璃酸钠或医用几丁糖。慢性持续疼痛影响情绪者,选用抗焦虑药物,改善抑郁、焦虑。中、重度疼痛患者慎用关节腔内注射糖皮质激素。中成药治疗OA的作用机制和长期疗效尚需高级别循证医学证据证实[49-51]。阿片类药物治疗OA并无明确权威性指南推荐,存在成瘾性、安全性等问题,不建议中度OA患者口服阿片类药物。
4.1.4 重度
患者疼痛严重,日常活动严重受限,经常出现关节肿胀,严重畸形。X线片显示关节间隙狭窄严重,骨赘形成明显,软骨下骨硬化、囊性变,关节畸形明显,K-L分级Ⅳ级。治疗方法包括关节置换,药物治疗以控制症状为目的。NSAIDs是缓解疼痛的首选药物,根据患者症状适当调整剂量,需警惕不良反应。优先考虑选择性COX-2抑制剂或同时服用PPI类药物以减轻胃肠道不良反应。鉴于阿片类药物的成瘾性和安全性等问题,不建议长期使用;择期手术短期或围手术期酌情使用。重度OA患者软骨破坏严重,延缓病情进展类药物和软骨保护剂作用甚微,不建议使用。此外,糖皮质激素对重度OA患者的严重疼痛作用甚微,不推荐使用。
4.2 不同个体用药的合理性
4.2.1 合并基础疾病
(1)心血管疾病:若存在严重心血管疾病和风险,需与心血管内科联合诊治,慎用对心血管疾病影响大的药物。选择心血管事件风险低的NSAIDs,如艾瑞昔布、塞来昔布、依托考昔等,并且使用小剂量阿司匹林加强心血管保护。OA合并高血压患者酌情使用艾瑞昔布、塞来昔布和依托考昔等,并规律服用降压药。同时监测血压,调整NSAIDs或降压药剂量。高血压患者服用NSAIDs后定期(每7~10天)复查肾功能。双醋瑞因可以抑制IL-1的促动脉粥样硬化作用,具有心血管保护作用且无明显心血管事件发生风险[12]。
(2)糖尿病:2型糖尿病(type 2 diabetes mellitus,T2DM)是老年患者常见疾病之一[52,53]。对于轻、中度OA所致疼痛,对乙酰氨基酚仍是一线用药,但应慎重选择对乙酰氨基酚治疗合并T2DM、晚期非酒精性脂肪性肝病、严重脂肪性肝炎等OA患者。同时建议糖尿病肾病高危患者慎重选择口服NSAIDs。局部外用NSAIDs应作为首选。双醋瑞因、玻璃酸钠、医用几丁糖等不影响T2DM患者体内葡萄糖代谢[54]。合理应用延缓病情进展类药物和软骨保护剂。
(3)消化道疾病:若存在严重消化道疾病和风险,需与消化内科联合诊治,慎用对消化道影响大的药物。NSAIDs可引起胃肠道刺激症状,如腹胀、恶心、胃灼热等,建议患者餐后服药,并服用抗酸药或组胺受体拮抗剂缓解症状[55]。相比于其他非选择性药物,选择性NSAIDs消化道溃疡发生率更低[56]。推荐米索前列醇或PPI(奥美拉唑等)用于预防高风险患者出现消化道溃疡等严重并发症[56-58]。组胺受体拮抗剂不推荐使用[58]。
4.2.2 肥胖
近年来,众多研究认为肥胖是OA重要的独立危险因素之一[59-61]。OA会增加肥胖、炎症及心血管疾病等发生风险[59,62]。患者宣教、自我管理、适当运动以及控制好体重是核心措施,建议在营养师、康复治疗师指导下控制好体重。
4.2.3 年龄
老年人是OA主要累及群体,且多对手术治疗有一定恐惧感,多数患者希望通过非手术治疗得到缓解,器官功能衰退和基础疾病亦增加了手术风险。因此,药物治疗对于老年OA患者尤为重要。根据疾病程度,内外结合,进行个体化与阶梯化治疗。
老年OA患者选用药物需注意:①因其不良反应发生风险更高,用药时应尽量使用最小有效剂量、缩短用药时间、局部用药,密切观察不良反应;②合并症较多,合并用药情况复杂,注意药物之间的相互作用;③密切关注病情进展情况,及时调整治疗方案;④老年人肝肾功能下降、代谢能力差,部分患者体重较轻,需酌情减量。
对于年轻的OA患者,多数为运动创伤导致,治疗原则是尽量延缓关节软骨的破坏,维持关节功能。年轻OA患者,及时去除诱发因素如半月板撕裂、游离体、关节内骨折、下肢力线异常等,及早使用延缓病情进展类药物和软骨保护剂,延缓关节软骨的破坏,维持关节功能。
4.3 疗程中的用药合理性
主要体现在安全性监测和有效性评估2个方面。
4.3.1 安全性监测
①患者每日自我评估;②医生用药随访评估;③餐后用药减少胃部不适;④避免超过每日最大剂量用药;⑤慎用非处方来源的对乙酰氨基酚药物;⑥长期用药存在肝毒性高风险者,应监测肝功能;⑦有肾脏疾病和使用影响肾功能药物(利尿剂、血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂等)的患者服用NSAIDs时,监测血肌酐和内生肌酐清除率,7~10 d评估肾功能;⑧NSAIDs镇痛治疗中国际标准化比值(international normalized ratio,INR)增高,监测INR,注意出血迹象,特别是既往有消化道溃疡或出血病史的患者;⑨合并高血压,在服用NSAIDs时测量基线血压,每2~4周监测1次,高血压未控制或服用降压药时,需要频繁监测血压(每1~2周);⑩避免使用2种及以上NSAIDs;服用低剂量阿司匹林进行心血管保护。
4.3.2 有效性评估
①疼痛与功能环节评估量表:视觉模拟评分法(visual analogue scale,VAS)量化和评估疼痛程度,美国特种外科医院(hospital for special surgery,HSS)评分、西安大略和麦克玛斯特大学骨关节炎指数(the Western Ontario and McMaster Universities osteoarthritis index,WOMAC)评分和膝关节学会评分(Knee Society score,KSS)评价活动能力(步行、锻炼、做园艺等);②患者每日自我评估;③医生用药随访评估;④如果疼痛控制满意,则继续当前用药方案,并找到最低有效剂量;⑤如果用药14 d后疼痛没有改善,改换备用药物;⑥如果对2种药物的治疗效果不佳,需要进一步评估;⑦如果疼痛正在改善但未达到最优,在确保最佳治疗(最大治疗剂量、定期给药等)情况下,考虑增加适当的辅助治疗(如局部镇痛剂等)。
4.4 合理用药的注意事项
①注意皮肤伤口、皮疹、感染等不良状况,慎用局部外用制剂;出现过敏反应,应及时停止使用。②对乙酰氨基酚过敏、严重肝肾功能不全者应禁用;摄入危险剂量酒精、老年人,剂量应减半;③个体化使用NSAIDs,使用最低有效剂量、缩短持续用药时间、尽量局部用药,必要时联合PPI;④消化道活动性溃疡和近期胃肠道出血、对阿司匹林或其他NSAIDs过敏、肝功能不全、肾功能不全、严重高血压和充血性心力衰竭、血细胞减少、妊娠期和哺乳期女性等患者,应禁用或慎用NSAIDs;⑤关节合并创伤、出血以及感染,禁用糖皮质激素,激素联用NSAIDs会增加消化道出血的发生风险;⑥关节内感染、穿刺部位皮肤破溃感染、注射部位附近或有全身感染、凝血功能异常、急/慢性出血性关节炎、损伤严重的创伤性关节炎、不能排除其他疾病引起的关节明显肿胀和积液,以及严重的关节变形或关节畸形者,禁止关节腔内注射玻璃酸钠或医用几丁糖;⑦双醋瑞因起效慢,治疗后2~4周显效,建议与其他镇痛药或NSAIDs联用;⑧慢性持续疼痛影响情绪者,选用抗焦虑药物,用药类型和剂量应在专科医生指导下选择;⑨作用机制类似的药物,不建议叠加使用,若效果不佳,则更换其他药物而非叠加,以避免增加不良反应。
05
骨关节炎临床药物治疗专家共识条目
(1)早期OA的非药物治疗非常关键,包括健康教育、控制好体重、合理锻炼、自我管理、物理治疗等。
(2)外用NSAIDs可作为OA早期药物治疗的首选,尤其适用于合并胃肠道疾病、心血管疾病或身体虚弱的患者,对小关节、肩锁关节、膝关节、肘关节等OA有效。
(3)口服NSAIDs适用于中、重度OA患者,推荐使用对胃肠道不良反应小的NSAIDs,但需警惕其心血管不良事件。
(4)由于阿片类镇痛剂的不良反应和成瘾性发生率相对较高,不推荐其作为OA镇痛的首选药物。
(5)糖皮质激素短期缓解OA肿痛效果显著,但不宜反复多次使用。
(6)关节腔内注射玻璃酸钠和医用几丁糖适用于轻、中度OA患者。
(7)关节腔内注射PRP适用于轻、中度OA患者。
(8)氨基葡萄糖对有症状的OA患者可选择性使用。
(9)在OA用药过程中,遵循能外用不口服、能口服不注射、能注射不手术的原则,依据OA不同程度,进行个体化、阶梯化的系统合理用药治疗。
06
结 语
有症状的OA必须治疗,尤其是药物治疗,其目的是缓解或消除疼痛症状,改善关节功能,延缓病情进展,提高患者生活质量。应根据患者个体特性、骨关节的部位、病情分期和程度,进行内外结合、个体化、阶梯化的系统药物治疗。在药物选择、联合用药、用药剂量和周期、用药注意事项、不良反应、安全性、有效性等方面均应做到合理化、科学性用药治疗。
利益冲突声明
所有参与本共识制定的专家对本共识有关的任何利益关系进行了无利益冲突声明,并填写了利益冲突声明表。
陈世益 复旦大学附属华山医院
王坤正 西安交通大学第二附属医院
陈世益 复旦大学附属华山医院
胡 宁 重庆医科大学附属第一医院
贾岩波 内蒙古医科大学第二附属医院
李 箭 四川大学华西医院
李 棋 四川大学华西医院
尚西亮 复旦大学附属华山医院
白伦浩 中国医科大学附属盛京医院
毕 擎 浙江省人民医院
陈世益 复旦大学附属华山医院
戴国锋 山东大学齐鲁医院
胡 宁 重庆医科大学附属第一医院
贾岩波 内蒙古医科大学第二附属医院
蒋 青 南京大学医学院附属鼓楼医院
靳英辉 武汉大学中南医院
李 箭 四川大学华西医院
李 棋 四川大学华西医院
李国平 国家体育总局运动医学研究所
林 朋 中日友好医院
刘 宁 郑州市骨科医院
刘玉杰 中国人民解放军总医院
吕 伟 黑龙江省医院
吕红斌 中南大学湘雅医院
尚西亮 复旦大学附属华山医院
孙 康 青岛大学附属医院
王 飞 河北医科大学第三医院
王 洪 华中科技大学同济医学院附属协和医院
王 青 南京医科大学第一附属医院
王健全 北京大学第三医院
王坤正 西安交通大学第二附属医院
卫小春 山西医科大学第二医院
伍 骥 中国人民解放军空军特色医学中心
邢更彦 解放军总医院第三医学中心
薛庆云 北京医院
杨 柳 陆军军医大学西南医院
余家阔 北京大学第三医院
郑 江 西安市红会医院





说明:本共识中不同厂家药物规格和剂量有所不同,使用前请详细阅读药品使用说明书或在药师指导下购买和使用。
声明:本文来源于医学前沿网(转载已授权),仅用于学习交流,不作任何商用!













