近些年,随着经济腾飞和生活水平改善,糖尿病与高血压患病率均不断升高。值得注意的是,在糖尿病病人中,高血压的患病率约为非糖尿病人群的2倍,并随年龄增长、体重增加及病程延长而上升,两种心血管风险相叠加,加速患者致残和死亡。本文主要介绍糖尿病病人合并高血压的发病机制、临床特征,以及治疗药物的选择。
一
糖尿病合并高血压的发病机制
糖尿病易合并高血压的机制较为复杂,概括为以下几方面:
①水钠潴留:高血糖可引起使细胞外液渗透压升高,从而引起细胞外液容量扩张。此外,高糖还使肾近端小管SGLT2表达增加,并刺激胰岛素分泌,而胰岛素可提高肾近端小管的SGLT2水平,以上均使肾近端小管重吸收葡萄糖增加, 因为SGLT2对葡萄糖的重吸收和对钠的重吸收是偶联的,所以在葡萄糖重吸收增加的同时,钠的重吸收也增加。
②RAS激活:高血糖可引起肾素、血管紧张素转换酶(ACE)和血管紧张素Ⅱ的I型受体
(AT1)表达增加,从而使RAAS激活。RAAS激活引起的醛固酮增加可使容量扩张,血管紧张素Ⅱ生成增加和AT1受体表达增加使血管收缩,这些均使血压升高。
③胰岛素抵抗和高胰岛素血症:胰岛素抵抗可使内皮细胞NO合成减少,还可使RAS系统和交感神经活性增加,从而使血压升高; 高胰岛素血症可导致交感神经活性增加并刺激肾素分泌,还会引起肾小管对钠的重吸收增加,这些均可使血压升高。
④自主神经紊乱:糖尿病可引起交感神经活性增加,使血管收缩、血压升高。交感神经活性增加还能刺激肾素分泌,间接使血压升高。
⑤其他因素:糖尿病还可引起血管内皮细胞功能紊乱,使得内皮源性缩血管物质(如内皮素)产生增加,而内皮源性舒血管物质(如NO)产生减少,从而使血压升高。
二
糖尿病患者启动降压治疗的时机
对正常高值血压患者(收缩压130-139 mmHg或舒张压80-89 mmHg),可通过生活方式干预来降压,若3个月后血压仍不达标,则开始服用降压药物治疗,但若已存在靶器官损害(如微量白蛋白尿或蛋白尿),应立即开始药物治疗。
若糖尿病患者收缩压≥140 mm Hg或舒张压>90 mmHg,除生活方式管理外,也应立即开始降压药物治疗。
三
糖尿病患者血压控制目标
基于循证医学结论,我国糖尿病合并高血压患者采取个体化管理策略,分层管理降压治疗的靶目标值:
①对于糖尿病病史较短、一般健康状况良好、无明显大血管病变且较为年轻的患者,血压控制目标为<130/80 mm Hg;
②对于高龄(65岁以上)、健康状况较差、已发生靶器官损害甚或伴严重冠心病患者,严格血压控制可能会因脏器血流灌注压不足而导致严重不良后果,可适当方宽到<140/90 mmHg;
③合并慢性肾病目标血压<130/80 mm Hg,如果尿蛋白≥1g/d时,则目标血压<125/75 mm Hg,透析患者目标血压为135/90 mm Hg。
四
糖尿病患者合并高血压的治疗
1.非药物治疗:
包括调整膳食结构、减少钠盐摄入、戒烟限酒、纠正不良生活方式、控制体重、规律适度的运动和心理疏导等。非药物疗法是降压治疗基本措施,不仅能降低血,而且能改善糖尿病患者的预后。
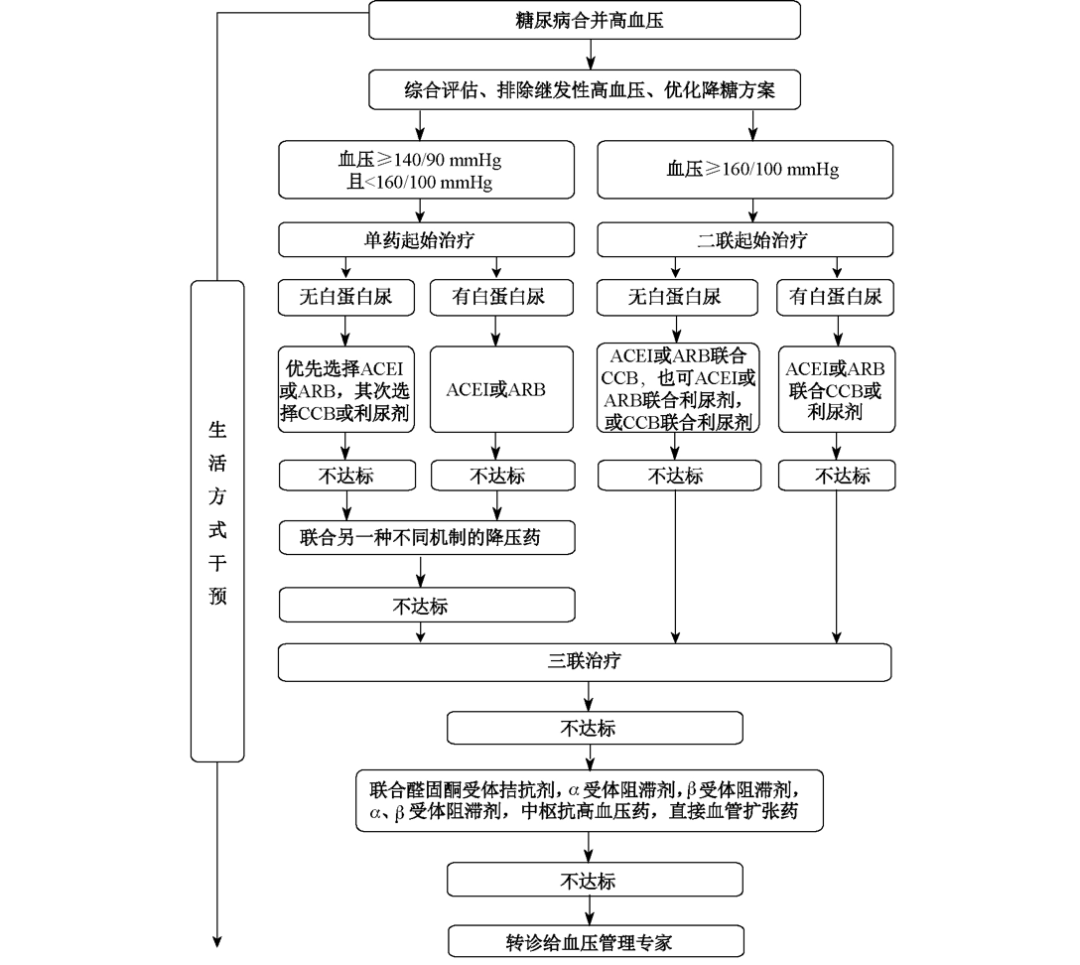
2.药物治疗
①ACEI/ARB类:为糖尿病合并高血压的首选降压用药。ACEI和ARB均有独立于血压水平的肾脏保护作用,在糖尿病肾病早期,可减少尿蛋白、延缓发展至终末期肾病(ESRD)进程,当肾功能衰竭时,该保护作用消失或减弱,内生肌酐清除率<30 ml/min时一般不再选用ACEI类药物。另外,合并双侧肾动脉狭窄和妊娠禁忌使用ACEI和ARB。
②β受体阻滞剂:通过抑制交感神经活性、减慢心率、抑制心肌收缩力发挥降压作用,尤其适用于伴快速性心律失常、冠心病、慢性心力衰竭、交感神经活性增高以及高血流动力状态(如甲亢)患者。
β受体阻滞剂对糖、脂代谢具有潜在不良影响且可能增加新发糖尿病的发生率,糖尿病合并高血压患者一般不首选β受体阻滞剂,必要时可慎重选用小剂量高选择性β1受体阻滞剂与ACEI或ARB联合治疗。
从靶器官保护角度,β受体阻滞剂与ACEI或ARB的联合可部分抵消β受体阻滞剂对糖代谢的潜在不利影响;β受体阻滞剂与长效二氢吡啶类CCB联合,可获得协同降压作用,同时抑制CCB引起的反射性交感神经兴奋;β受体阻滞剂与非二氢吡啶类CCB联用可诱发或加重缓慢性心律失常和心功能不全,应注意避免。
β受体阻滞剂与利尿剂联合应用可能对糖代谢产生不利影响,应尽量避免。另外,高度房室传导阻滞、哮喘患者为禁忌证,慢性阻塞型肺病、运动员、周围血管病慎用。
③CCB类:通过阻断血管平滑肌细胞钙离子通道发挥扩张血管降低血压的作用,对代谢无不良影响。降压作用不受高盐饮食影响,尤其适用于我国盐敏感性高血压。
CCB类可与其他四类降压药联合应用,常见不良反应包括反射性交感神经激活致心悸、面部潮红、踝部水肿等。
CCB包括两个亚类,即二氢吡啶类CCB和非二氢吡啶类CCB;其中二氢吡啶类CCB慎用于心动过速与心力衰竭患者,非二氢吡啶类CCB避免用于房室传导阻滞、病态窦房结综合征和左室收缩功能不全的老年糖尿病患者。
④利尿剂:通过利钠排尿、降低高血容量负荷发挥降压作用。包括噻嗪类利尿剂、袢利尿剂与醛固酮受体拈抗剂等。
肾小球滤过率估计值(eGFR)≥30 ml/min/1.73 m2时选用噻嗪类利尿剂,eGFR<30 ml/min/1.73 m2时选用袢利尿剂。
大剂量噻嗪类利尿剂应用可致糖脂代谢紊乱、电解质失衡、高尿酸血症和肾脏血流灌注受损。由于利尿剂对糖尿病患者的综合影响尚有待更多论证,因此不推荐将此类药物作为糖尿病伴高血压患者的一线治疗。
⑤α受体阻滞剂:不推荐作为糖尿病合并高血压患者常规治疗,仅对重症或顽同性高血压,应用ACEI/ARB、CCB和利尿剂治疗后血压仍不能达标或不能耐受的2型糖尿病患者,可考虑联合应用此类药物。
不良反应主要是体位性低血压,治疗应使用控释制剂,从小剂量开始,睡前服用,依据患者治疗反应逐渐增加剂量,并监测立位血压。
⑥联合降压药物治疗:研究表明,超过70%糖尿病患者需要2种或2种以上不同种类的降压药物联合治疗。联合用药的优势在于密切关注患者心血管危险因素以及靶器官损害情况基础上,应用多种不同机制联合降压,同时抵消不良反应,更有利于靶器官保护。

对于血压明显升高或高危的糖尿病合并高血压患者,ACEI/ARB与CCB联合治疗有利于改善血管内皮功能,发挥更强的抗动脉粥样硬化作用,ACEI/ARB可阻断CCB所致反射性交感神经张力增加和心率加快的不良反应 同时扩张静脉改善回流,减轻踝部水肿,推荐启动阶段以ACEI/ARB为基础的联合治疗;若血压仍不能达标,可在此基础上加用小剂量噻嗪类利尿剂,此时可减弱利尿剂对肾素一血管紧张素一醛同酮系统激活的不利因素;若患者存在冠心病或心力衰竭等并发疾患,可考虑联合使用选择性β受体阻滞剂。
参考文献:
1.中华医学会糖尿病学分会.中国2型糖尿病防治指南(2020年版)[J].中华内分泌代谢杂志,2021,37(04):311-398.
2.国家卫生健康委员会能力建设和继续教育中心.糖尿病患者合并心血管疾病诊治专家共识(2021版本).中华内分泌代谢杂志,2021,60(05):421-437.
3.上海市医学会糖尿病专科分会.成人糖尿病患者血压管理专家共识[J].上海医学,2021,44(01):8-18.
4.中华医学会内分泌学分会.中国糖尿病患者血压管理的专家共识[J].中华内分泌代谢杂志,2012(08):614-618.

声明:本文为原创内容,作者yuki,仅用于学习交流,转载需授权。内容仅代表作者个人观点,望大家理性判断及应用。