经导管主动脉瓣植入术(TAVI)已逐渐发展普及为一种常规介入治疗,其相关的并发症是影响患者预后的重要因素,需要及时发现并积极处理。本文将介绍TAVI常见并发症之一——瓣周漏及其危险因素、预防和治疗原则,帮助认识与管理TAVI常见并发症。
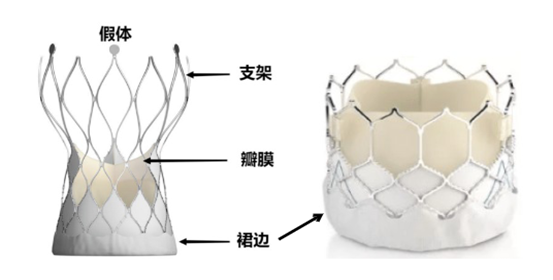
瓣周漏(PVL)是指人工瓣膜与自体主动脉根部未完全贴合,导致血液从其中缝隙反流至左心室的现象。在TAVI早期开展的时候,是较为常见的并发症,但随着评估策略和新一代瓣膜的改进,重度PVL发生率降至约3%以下。
研究显示,中度以上PVL可增加再入院、心功能恶化、短期和长期死亡风险;轻度PVL也可能不利于预后;而微小PVL可能由于机械性作用而引起溶血。故PVL应尽量避免,及时处理,并密切随访观察。
危险因素与预防策略
-
PVL的危险因素
TAVI手术本身不切除原生瓣膜,且植入的人工瓣膜并非缝合固定在主动脉根部。因此其定位、膨胀与固定易受主动脉根部形态和组织结构等因素影响,从而导致人工瓣膜在某些解剖情况下(如瓣叶严重钙化/纤维化/粘连等)可能出现不完全贴合瓣环的情况,从而出现PVL。此外,瓣膜位置不佳,植入过深、过浅,也会影响人工瓣裙边对瓣环的密封性,进而产生PVL。
解剖因素
瓣环及左室流出道(LVOT)钙化严重或有巨大钙化团块、钙化分布不对称;巨大瓣环;二叶式主动脉瓣;横位心导致瓣膜同轴性欠佳,往往无冠窦侧瓣膜植入过浅。
02
器械因素
使用初代瓣膜;与球扩瓣相比,自展瓣发生轻度手术因素:瓣膜尺寸选择过小;瓣膜扩张不足;瓣膜植入过浅或过深。
03
术后因素
人工瓣膜心内膜炎,主要特征为瓣膜赘生物形成,导致瓣膜结构破坏和功能受限。
-
PVL的预防策略
① 选择合适型号的瓣膜,保有一定的oversizing率。
② 使用可回收的瓣膜输送装置。
③ 使用有裙边等防护结构的人工瓣膜。
④ 准确定位瓣膜的植入深度。
⑤ 在预防人工瓣膜感染性心内膜炎方面,需要注意手术无菌操作,可予以预防性应用抗菌药物,术后监测体温变化,关注感染症状。
评估与诊断
准确测量PVL严重程度对于判断TAVI手术效果及处理策略具有重要的意义,主要的评估方式为主动脉根部造影和心脏彩超。
主动脉根部造影可在TAVI术中直观显示主动脉瓣反流情况,但难以区分反流来自人工瓣中心或是瓣周。应在撤出导丝后进行评估,以免导丝阻挡瓣叶使其关闭不良从而造成误判。造影时需要注意猪尾导管应靠近主动脉瓣,不应过高,以免低估反流程度,图像记录应当持续至造影剂从主动脉根部排出。
通常使用Sellers视觉分级量表进行粗略量化,将反流程度分为四个等级:
-
0级:无AR。
-
1级:舒张期少量造影剂进入左室,未充心腔,可在每个心脏周期中被清除。
-
2级:在舒张期,反流的造影剂充满左室,但密度低于升主动脉。
-
3级:在舒张期,反流的造影剂充满左室,密度与升主动脉相同。
-
4级:在舒张期,反流的造影剂充满左室,密度高于升主动脉。
心脏彩超不仅能够量化评估PVL严重程度,还能显示PVL发生部位和形态,以及是否合并血栓、赘生物等。以下是PVL三级分类的超声评价标准。
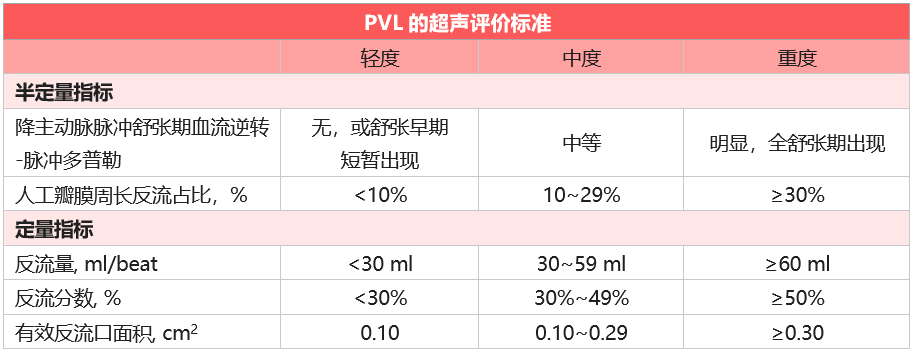
治疗原则
对于不同的情况和PVL原因,需要选择不同的处理策略。较大的PVL难以自发闭合,且不利于预后,需要积极处理。
在术中怎么办?
术中若使用可回收瓣膜,可在部分释放时重新回收,及时纠正瓣膜定位不良。若人工瓣扩张不充分,可使用球囊后扩张,依据术前CT选择适合主动脉根部平均直径的球囊尺寸,以避免过度球囊扩张引起瓣环破裂。若人工瓣植入过深且无法重新回收,可尝试用网篮捕获人工瓣膜边缘,逐渐向主动脉侧拉动,但要防止使瓣膜移位导致栓塞,且若瓣膜边缘朝向主动脉壁,有主动脉夹层的风险。当人工瓣植入过深或过高时,也可考虑植入第二个人工瓣膜。
若PVL的面积相对较小,使用封堵器可能是有效的选择。
对于情况危急的严重PVL,可考虑外科手术补救。对于感染性心内膜炎所致的人工瓣膜PVL,首选外科手术治疗。
-END-
声明:本文转载于<中国医学论坛报今日循环>,作者:四川大学华西医院 姚怡君。仅用于学习交流,版权归原作者所有。













