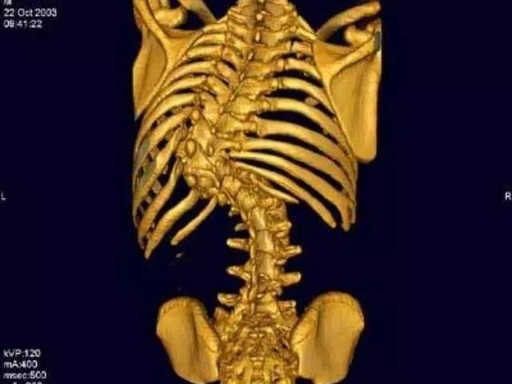
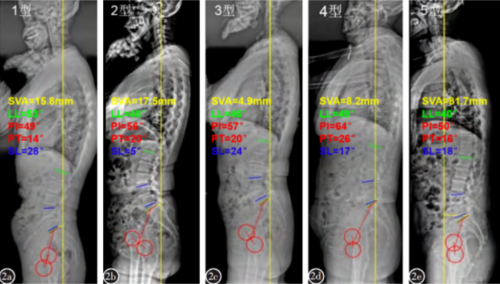
前言
胸椎椎体切除术是用于治疗伴有椎管损伤的外伤性、感染性、发育不良性和肿瘤性椎体骨折等手术方法。传统上,这种手术的后外侧入路需要切除入路侧多达 6 厘米的肋骨,以便从足够外侧空间进入切除椎体,从而到达前柱,避免胸椎脊髓的过度牵拉。然而,这种肋骨切除已被确定为术后并发症的主要原因,包括切除部位疼痛和随之而来的呼吸限制、高额住院费用和潜在的术后并发症。最近对该方法进行了改进,利用肋骨固定术(即肋骨成形术)将病灶肋骨不稳定引起的疼痛降至最低,对术后疼痛和住院时间(LOS)产生了积极影响;但是,仍然需要在肋骨明显不稳定的情况下进行横断,并在侧卧位进行手术。使用较少侵入性且保留肋骨的手术技术被证明可以有效减轻非脊柱手术后的疼痛,例如在显微外科乳腺重建中进行的内部乳动脉血管采集及用于肾脏移植的小切口供体肾切除术。此外,超声骨手术刀(UBS) (Misonix, Farmingdale, NY, USA)在脊柱外科医生的器械中应用,与一些系列的传统方法相比,已被证明能够减少失血、神经损伤、手术时间和骨质流失。我们提出了一种先前描述的技术,该技术结合了这些原则,使用UBS实现了肋骨保留胸椎体切除术。
手术技术说明
患者俯卧在Jackson框架上,放置胸垫、臀垫和平膝板。神经监测用于监测体感诱发电位(ssep)和运动诱发电位(MEPs),以检测神经根和潜在硬膜囊操作过程中神经损伤的任何早期迹象。在中线进行的骨膜下剥离,在病椎水平(CL)暴露胸椎后部以及头尾两侧的2 ~ 3个椎体,以便进行节段内固定。该技术的这一部分可以修改为“小切口”,根据需要进行单一中线筋膜外剥离。当切开时,在CL在肋横关节的外侧进行,以暴露在计划的入路侧的内侧肋骨几毫米。在CL上方和下方选择的椎弓根在两侧进行准备,但此时只在对侧放置椎弓根螺钉。在小开口型椎弓根螺钉中,经皮椎弓根螺钉可以使用常规的套筒、k针和空心螺钉系统组合置入。然后,可以开始进行切开术。
我们倾向于使用 UBS 进行整体椎板切除术。通常需要切除部分或全部棘突和椎体上部的下层椎板,以获得足够的视野和最大的工作角度。UBS 用于切除 CL 下关节突的整个部分和侧上方的椎体。然后,以同样的方式切除CL上关节突的最上部分和下面的椎体,注意不要破坏椎弓根。然后在入路侧切除CL横突的根部,以放置人工椎体,留下足够的骨以避免肋横关节脱位。如果需要额外的角度调整,肋横关节可能会在这一操作过程中脱位,但重要的是,肋骨本身不会受到损伤。这些截骨术会导致孤立的椎弓根。使用咬骨钳咬除骨头,直到看到基底的松质骨。在极少数情况下,胸肋骨角度可能过于陡峭,无法采用我们的技术;在这种情况下,可能需要转换为更传统的肋横切术。在这一点上,我们更倾向于结扎,然后分离出口神经分支近端背根神经节,以最大限度地扩大手术通道。标记的神经根可以通过缝合和一个小钳的重力牵拉。在入路的对侧放置一根临时杆,用于矢状面稳定。在CL上方和下方按标准方式进行椎间盘切除术。然后,使用盒形截骨器去除剩余的椎弓根柱,直到与后椎体齐平。我们更倾向于使用相同的器械通过创建的通道进行椎体切除术,因为我们发现这是取出椎体的有效方法。保留前皮质边缘保持完整,以防止融合器移位。垂体钳用于切除骨性碎片。接下来,使用Woodson来确认硬膜囊腹侧与剩余的后纵韧带和后椎体之间的分离情况。在翻修手术或感染性肿瘤适应症需要进行胸廓切除术的病例中,术前通常会预计到硬膜外纤维化,并采用标准的显微外科技术将硬膜与周围结构分离。先天性硬脑膜缺损要根据具体情况进行处理,首选进行初次缝合修复。如果初次修复无效,则可结合使用填塞物、各种合成衬垫、密封剂、对缺损进行强力软组织覆盖以及纯重力引流系统。先用一个反角刮刀刮出一个空腔,将剩余的后壁骨块用足跟型顶棒打入空腔,并将骨块移除。
使用 USB 对椎体外侧皮质进行刮除,刮除量仅为椎体笼导入所需的空间(图 1)。由于保留了这一侧皮层,肋骨中心的衔接处以及肋骨本身就不会受到影响。这种技术的关键在于使用可扩展的人工椎体,可以通过适当的尺寸、放置和扩展来实现所需的前柱重建。为此,我们更倾向于使用带有模块化端盖的人工椎体(VLIFT→,Stryker, Kalamazoo, MI, USA)。在引入融合器时,无需将硬膜囊牵开至标记神经所达到的最小旋转角度之外(图2)。随后使用标准的程序完成手术。
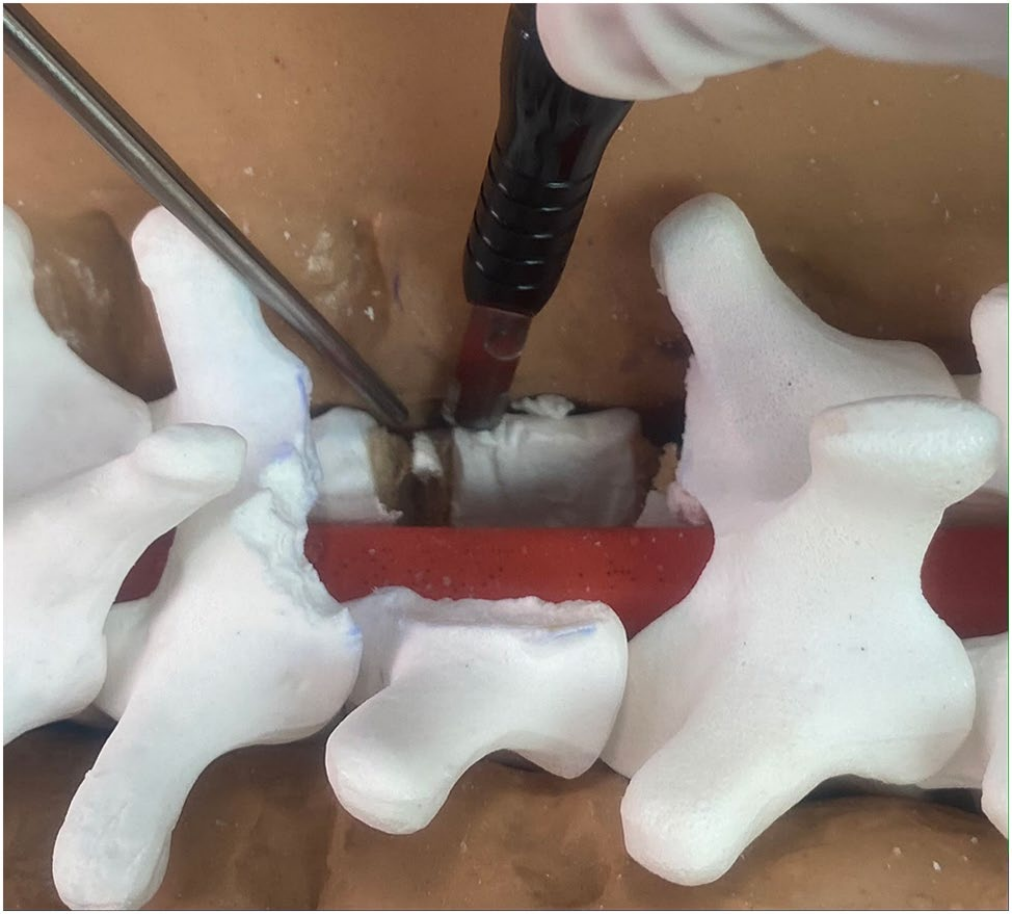
如图1所示,超声骨刀的精细尖端可以精细地调整椎体侧方的宽度,而不是像在这个塑料脊柱模型上所展示的那样进行整体切除。
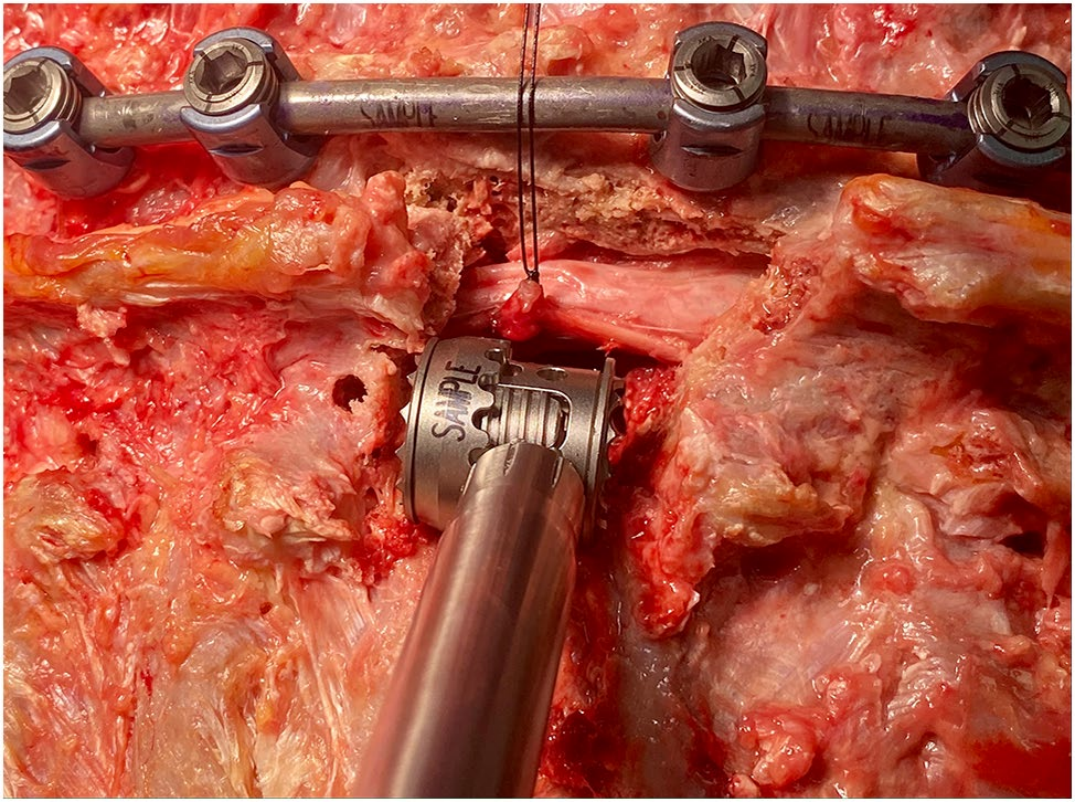
如图2所示,在这具尸体标本中,人工椎体被放入预先截好骨的骨窗中,仅使用标记的神经进行轻柔的牵引。
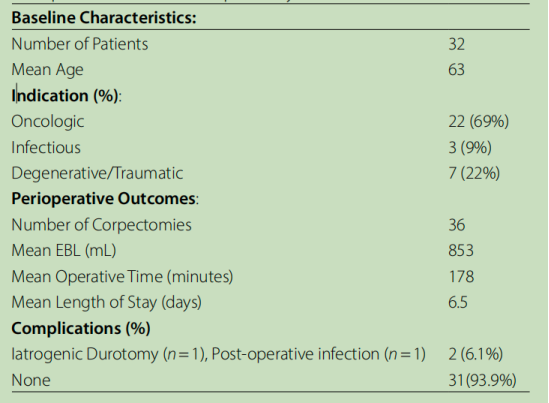
2015年8月至2023年3月,共对32例患者进行了36例椎体切除术(表1)。患者年龄从17岁到85岁(平均63岁)。最常见的适应症是肿瘤(n= 22,69%),其次是退行性/外伤性畸形(n= 7,22%)和感染(n= 3,9%)。在可访问数据的30/32例病例中,EBL平均为853 ml。有数据的29/32例的平均OT为178分钟。所有病例术后平均LOS为6.5天。发生1例医源性硬脊膜撕裂(3%),为术中唯一并发症,一期修复后无临床后果。只有一名患者(3%)出现手术并发症:手术部位感染,三周后需要清洗伤口,不需要进行内植物翻修。该患者的其余康复过程并无异常。另有一名患者在家庭康复期间摔倒,导致人工椎体刺入尾侧椎体骨折,因而需要进行手术修复以实现神经减压和脊柱稳定。这一异常事件被认为与手术本身无关。
表1 接受保留肋骨单侧经椎弓根胸椎椎体切除术患者的基本特征、手术指征和围手术期结局。
案例分享
【案列1】
一位70多岁的女性因进行性、难治性机械性背痛到医院就诊。经放射学检查,发现该患者存在弥漫性骨转移,且未发现原发性癌症。她有多处脊柱病变。最大的病变位于 T8 椎体水平,造成了轻微的病理性骨折(图 3)。肿瘤生长至后方结构和硬膜外间隙,造成严重脊髓压迫。与患者及多学科肿瘤团队讨论后,决定为她进行右侧保留肋骨的经椎弓根T8椎体切除术,以进行组织病理学诊断,并整块切除肿瘤,旨在保留神经功能,同时进行前柱重建和机械稳定(图4)。她的病情并不复杂,术后神经系统依然完好。出院后,她接受了康复治疗和门诊治疗,结果发现她是浆细胞肿瘤。
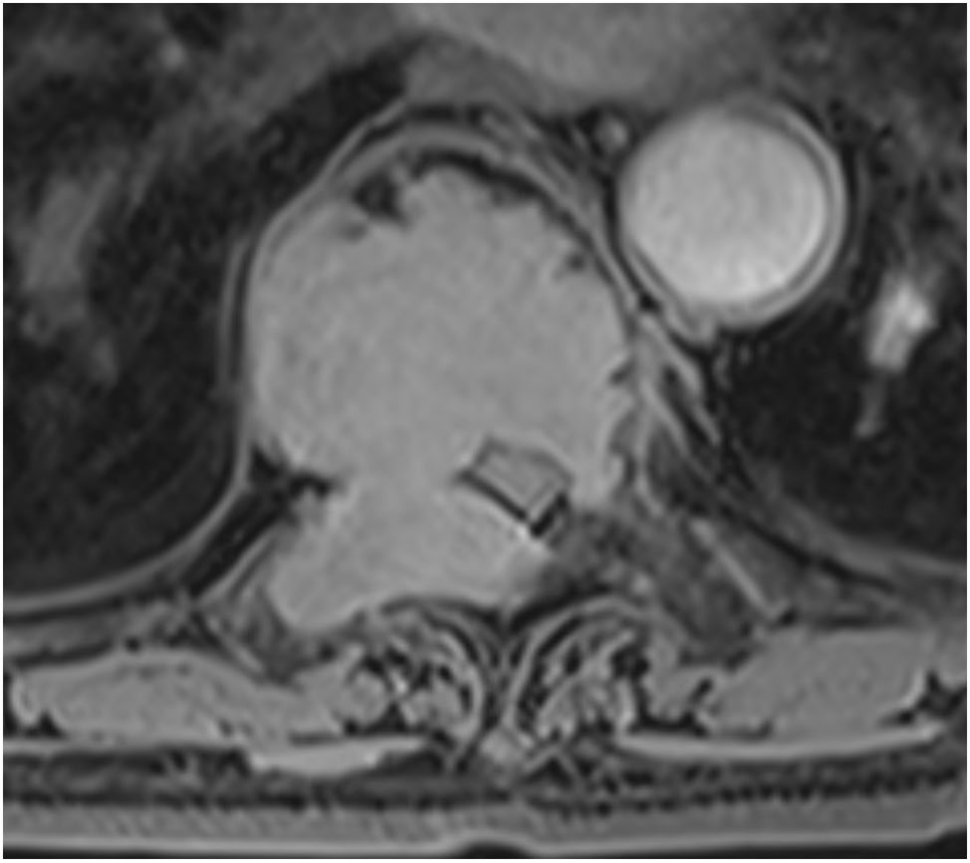
图 3 一位老年女性胸椎增强 T1 加权后轴向图像,显示 T8 处有一个均匀增强的肿块,病理特征与浆细胞瘤一致。
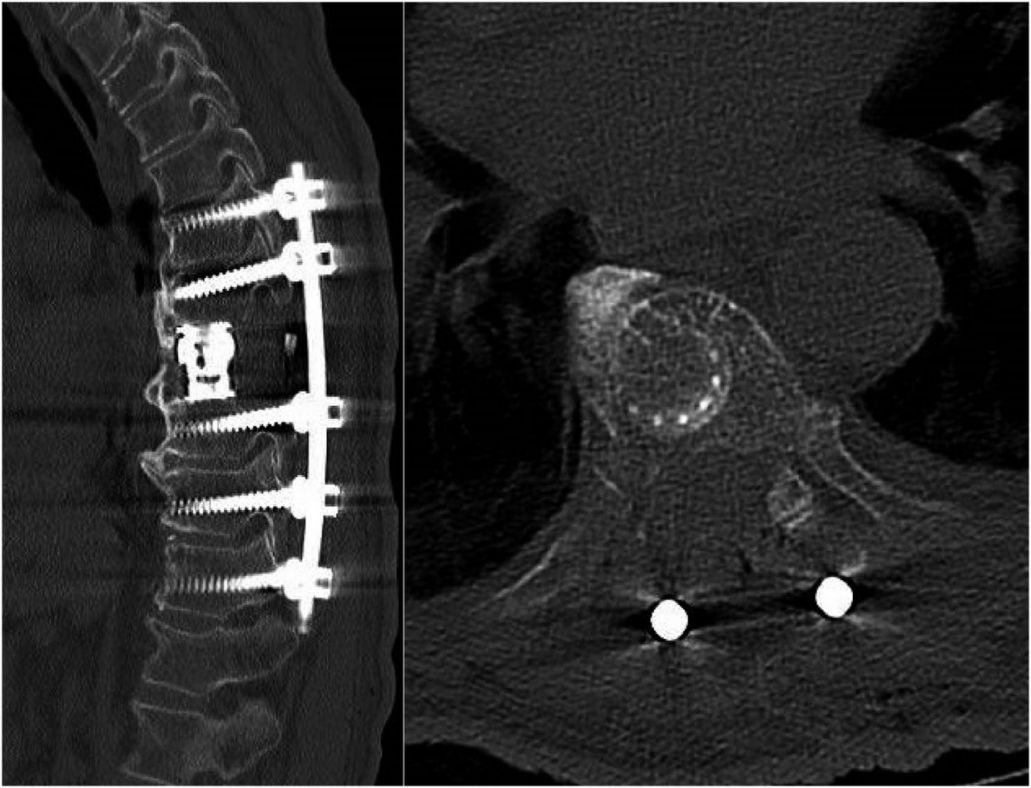
图4 患者术后CT扫描的矢状面(左)和轴面(右)切片,分别显示经椎弓根入路侧的矢状面前柱重建和完整的肋椎关节。
【案例2】
一名80多岁的男性患者,尽管接受了适当的静脉抗生素治疗,但仍持续存在耐甲氧西林金黄色葡萄球菌菌血症,以及T3和T4椎体椎间盘骨髓炎伴急性脊柱后凸畸形、骨性后突和硬膜外脓肿,表现为顽固性上背部疼痛,导致患者卧床不起(图5)。考虑到患者病情持续恶化,生活质量迅速下降,且无神经学缺损,为控制感染源、缓解机械性背痛、保护神经功能并矫正其矢状面畸形(见图6),对其施行了左侧保留肋骨的经椎弓根T3和T4椎体切除术。值得注意的是,T4椎体的外侧皮质因慢性感染而受到侵蚀;尽管如此,在手术入路过程中仍能够保留剩余的肋骨头。患者病情并不复杂,术后机械性背痛得到缓解,并未出现呼吸疼痛。他出院后被送往一家专业护理机构,神经系统完好,疼痛得到控制,可以继续接受门诊抗生素治疗。
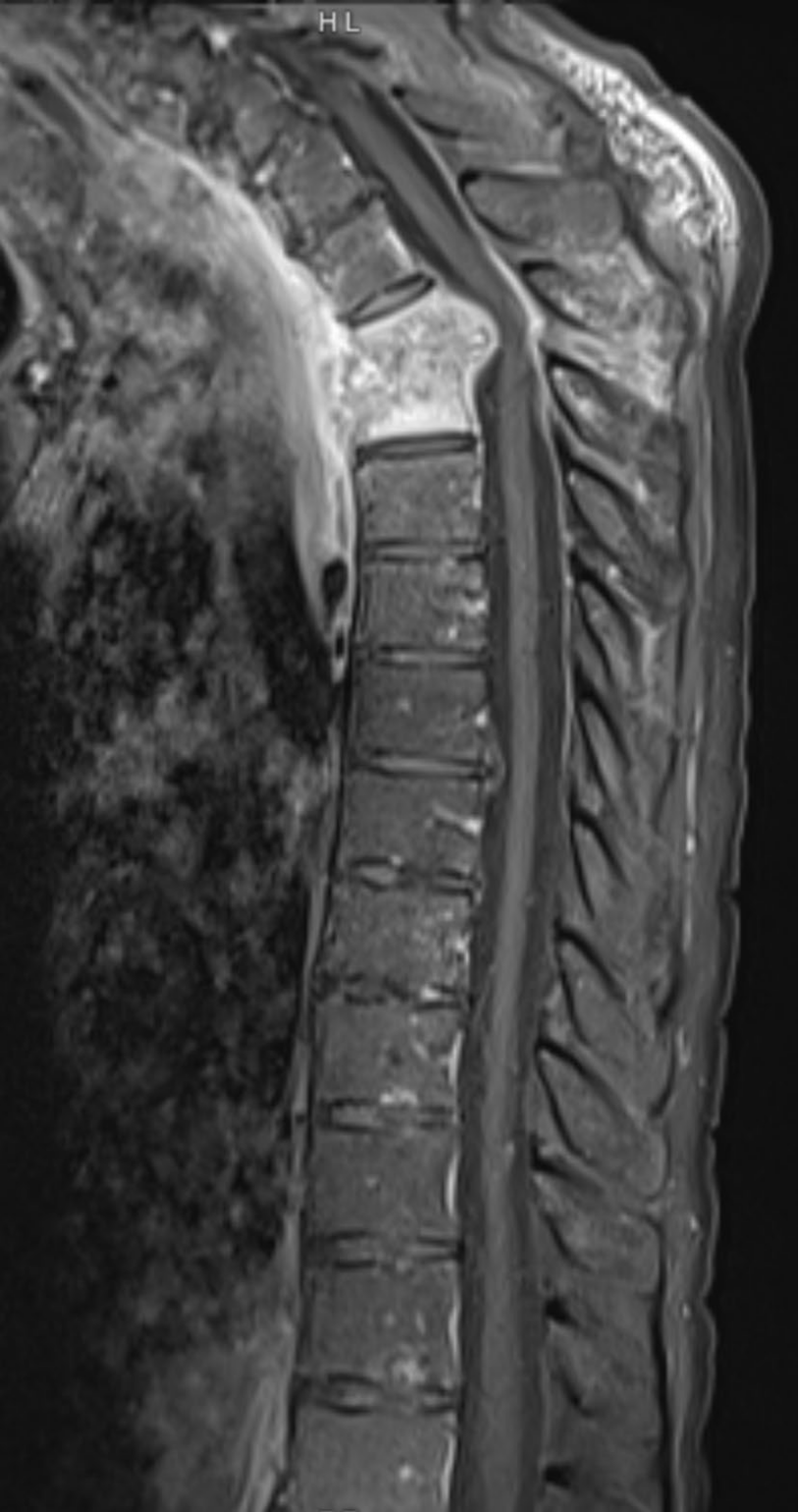
图5为一名老年男性的脊柱,显示T3椎间盘骨髓炎,以及胸椎T4椎体钆剂增强后的矢状位T1加权图像,可见急性脊柱后凸畸形、骨性后突和硬膜外脓肿。
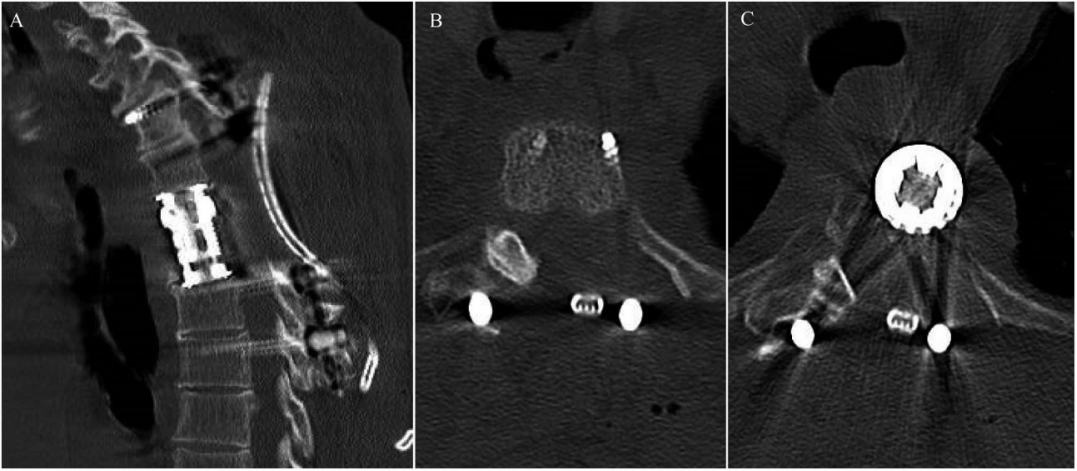
图6 患者术后CT扫描的矢状位(A)、轴位T3水平(B)和轴位T4水平(C)切片,显示了两个水平的矢状前柱重建和经椎弓根入路侧未切除的肋骨头。术前,T4侧椎体已受感染侵蚀。
讨论
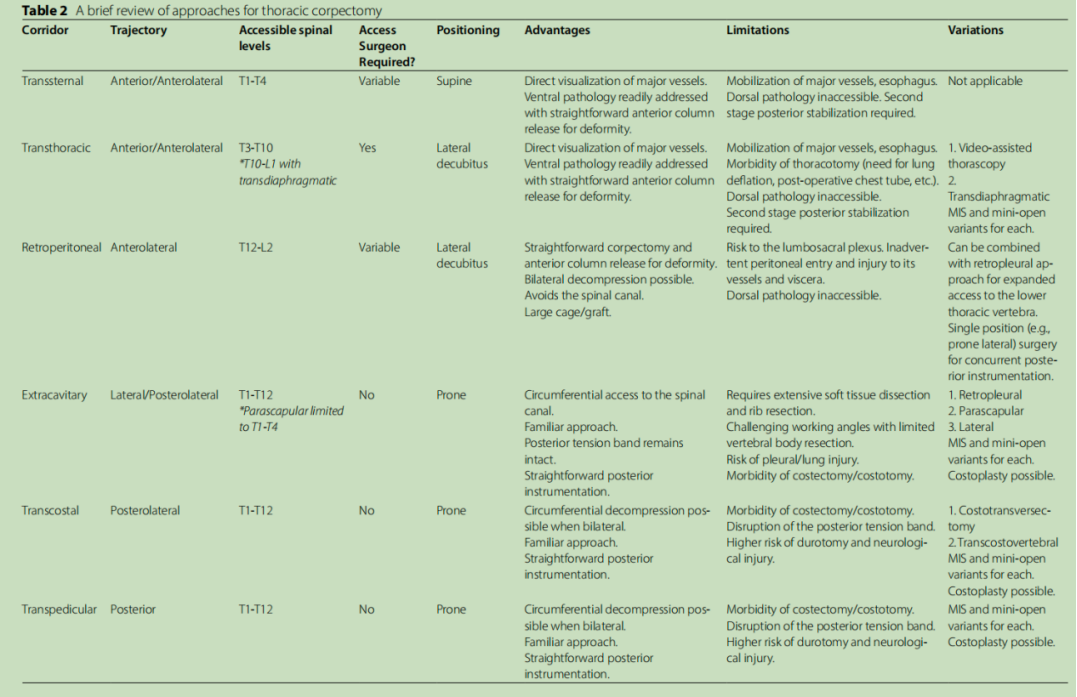
有几种很好的胸椎病理方法。这些包括,从前到外侧到后,经胸骨,经胸,经腹腔,腔外外侧腔外,肋横和经椎弓根通道。这些方法中的许多都有变体,每种方法都有其优缺点以及固有的局限性,这些都已经过先前的研究和描述(表2)。在后路手术中,主要的限制和挑战在于接近椎体的陡峭倾斜度,这需要对肋骨进行不同程度的切除以适应足以进行人工椎体前柱重建。通常,取出的肋骨被用作自体移植物,一些作者认为这在一定程度上抵消了其切除带来的发病率。
与本文所述技术最接近的是Dihn等人和Roy-Camille最初描述的经肋椎关节和经椎弓根入路。我们的技术融合了这两种方法的原理。与经肋横入路一样,在极少数情况下,我们需要去除后肋皮质以适应特别陡峭的后关节。不过,与这种方法的原始描述不同,我们的方法并不局限于椎间盘病变。作者之间的细微差别仍然存在,但目前所描述的经椎弓根胸椎体切除术方法仍需要长达6厘米的肋骨切除术或肋骨切开术,以便植入移植物或人工椎体。微创管状牵开器已尝试减轻由经椎弓根入路所需的软组织剥离引起的发病率,且效果良好。该领域的专家同样为此描述了铰链式肋骨成形术技术。虽然这确实能改善术后发病率,但也可能增加手术的复杂性和手术时间。这种经椎弓根的胸椎椎体切除术技术通过避免操作、去稳定或切除相应的肋骨头,从而避免了上述的发病率。
肋骨切除与显著的围术期和术后疼痛相关,这一事实在心血管胸外科文献中有广泛记载。此外,由于肋骨切除范围广,手术时间长和围术期大量失血都会增加术后并发症的风险。围术期疼痛加剧,加之切除肋骨可能引发的其他并发症,如胸膜损伤、血气胸或术后需置入胸腔引流管,均可延长接受侧方、后外侧及后方胸椎椎体切除术患者的住院时间。据文献报道,涉及大范围肋切除的后路胸椎椎体切除术的平均住院时间为10.5天。与文献相比,术后我们的患者平均节省了4.0天。同样,疼痛控制的改善也有利于患者恢复,因为快速活动和康复减少了与长期卧床相关的长期并发症。
研究传统开放性后路胸椎椎体切除术的报告称,平均估计失血量(EBL)为1687 ml,手术时间为357分钟,并发症发生率高达21.1%。自将超声骨刀(UBS)引入该技术以来,我团队平均手术时间为178分钟,预估失血量(EBL)为853毫升,与文献相比,有效地将预估失血量和手术时间减半。该工具易于使用,具有相对组织选择性,去除骨质有限,并且能够凝固松质骨滋养血管,从而使得(甚至可以说实现了)我们的胸椎椎体切除术变得简便易行。这些技术改进既可以缩短手术时间,又可以减少对输血的需求,并可能促进早期关节融合——这一发现已被该技术的其他采用者所证实。由于超声骨刀优先切割非弹性组织,因此能够降低医源性硬膜损伤的发生率(1.5–5.7%),这一点深受外科医生们的欢迎。鉴于Todeschi等人进行的前瞻性随机试验,这一点尤其突出。该试验表明,与单阶段后路一期手术相比,分阶段外侧椎体切除术治疗胸腰椎爆裂性骨折导致的硬脊膜撕裂更少。在我们仅采用后路技术的系列研究中,仅有一名患者(3%)出现了医源性硬脊膜破裂。历史上也曾有技术描述保留了肋横突关节,但在这些案例中,使用的是Steinmann针和骨水泥进行重建,这样形成的通道更狭窄。肋骨成形术、肋骨切开术或肋骨切除术的指征取决于需要创建一个足够大的通道,以便进行椎体切除术,以及随后从后外侧放置人工椎体和重建前柱。鉴于上述手术步骤所创建的骨窗相对较小,因此必须使用相应较小的植入物。可伸展的人工椎体是我们技术的必要条件。一些团队已经报道了他们使用模块化人工椎体的经验,这些人工椎体具有较高的关节融合率,能够恢复矢状位的垂直对齐,且使用方便。几十年来,人们一直知道,在进行前路椎体融合器重建后,需要进行额外的后路稳定,以增加结构的刚度,从而保持畸形矫正并防止移植物下沉。考虑到钛与松质骨之间弹性模量的较大差异,在使用我们偏好的钛合金内植物,这一概念尤为重要。值得注意的是,尽管我们通常不在这项手术中使用导航,但有些团队发现,在立体定向引导下放置人工椎体时,人工椎体错位率更低,从而减少了下陷的情况。
本研究的一个主要局限性在于使用医院住院时长(LOS)作为直接疼痛评分结果的替代指标,而在研究期间并未正式收集直接疼痛评分。与其他胸椎椎体切除术相比,我们的技术主要优势在于肋椎关节,甚至肋横突关节的稳定性。然而,该技术适用于中度畸形病例,可能不适用于严重畸形病例,因为在严重畸形病例中,为实现前柱重建,还必须切除最前侧和最外侧的椎体皮质,例如:驼背畸形、晚期库梅尔病、强直性脊柱炎、克利佩尔-费尔异常或夏科氏脊柱关节病。例如:gibbus畸形、晚期Kummell病、强直性脊柱炎、Klippel-Fiel畸形或Charcot脊柱关节病。在此类情况下,确实可能需要通过离断肋骨或切除肋骨来实现所需的矫正。我们的技术对于术后椎体切除术疼痛的改善理论应通过正式的疼痛评分记录或对术后止痛药使用情况的细致追踪来验证。此外,有必要在多个机构和更大队列中进行进一步的前瞻性研究,以推荐将此技术应用于日常临床实践。
结论
在大多数脊柱外科医生所熟悉的单阶段后路单侧经椎弓根入路中,结合使用UBS(通用脊柱系统)和模块化可扩展融合器,可以有效地实施保留肋骨的胸椎椎体切除术。该技术可能会减少因其他入路所需肋骨操作而导致的术后发病率。对术后疼痛控制进行前瞻性定量研究,包括患者报告的评分和止痛药使用情况,可以进一步验证这一假设。
文献来源:A rib-sparing unilateral transpedicular thoracic corpectomy using the ultrasonic bone scalpel: a novel technique and pictorial guide(请以原文为准,中文仅供参考)https://doi.org/10.1186/s12893-024-02602-0
声明:本文为原创内容,作者杨海平,观点仅代表作者本人,仅用于学习交流,未经授权禁止转载!