摘 要
电风暴是一种独特的医疗紧急情况,它引起机体大量分泌儿茶酚胺,从而导致恶性心律失常,表现为反复发生的室速或室颤,死亡风险大大增加,此时通常需要电复律及电除颤等紧急治疗。目前主要治疗措施包括病因治疗、电复律或电除颤、镇静、药物、植入式心脏复律除颤器、导管消融等。
电风暴(electrical storm,ES)又称心室风暴、儿茶酚胺风暴、交感风暴,特征是为在24h内由三次或多次发作的持续性室性心动过速(ven-tricular tachycardia,VT),室颤(ventricular fi-brillation,VF),或者引起植入式心律转复除颤器(implantable cardioverter defibrillator,ICD)的治疗。2014年《EHRA/HRS/APHRS室性心律失常专家共识》将ES定义为“24h内发生≥3次明确需要抗心动过速起搏(antitachycardia pacing,ATP)或电除颤治疗的VT/VF”。一项荟萃分析表明,ES导致死亡风险增加了近3倍。
一、电风暴的病因和机制
(一)病因
ES是多种病因及诱因的综合作用,可发生在各种环境下,按基础疾病可分为心脏性疾病和非心脏性疾病,在心脏性疾病中,包括心肌梗死、严重瓣膜病、缺血性或非缺血性心肌病以及先天性传导异常,如Brugada综合征或Wolf-Parkinson-White综合征。其中以急性冠脉综合征的发生率最高,且随着ICD在临床中的广泛应用,ES的发生率也随之增高。很多非心脏性疾病,包括创伤后应激综合征、急性肾脏衰竭、急性出血性脑血管病、慢性阻塞性肺疾病、病毒感染等均可引起ES。
(二)发病机制
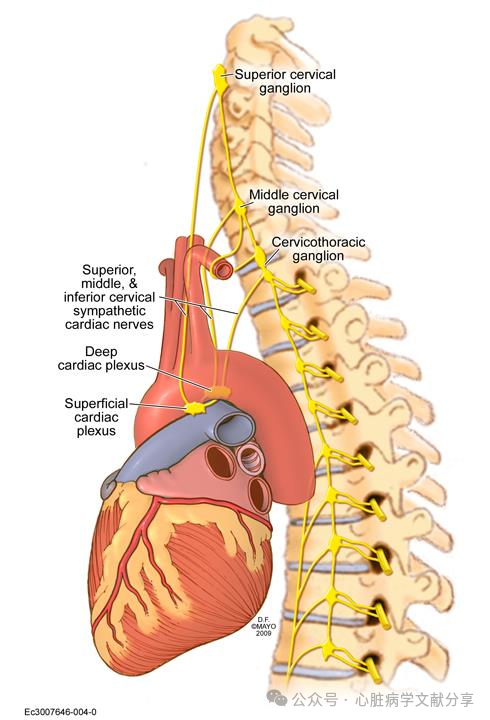
ES是内环境、电生理和自主神经系统改变等多种因素综合改变所致,其机制尚未完全明了,目前主要认为交感神经过度激活、β受体反应性增强、希氏-浦肯野系统传导异常所致。
1.交感神经过度激活 交感神经过度激活贯穿整个ES,当机体受到内外界环境及心理因素刺激时,交感神经激活,血浆中去甲肾上腺素等儿茶酚胺大量释放,去甲肾上腺素与心肌β-肾上腺素能受体结合,后者通过刺激性鸟嘌呤核苷酸结合蛋白Gs与腺苷酸环化酶细胞内连接。腺苷酸环化酶的刺激增加了细胞内第二信使环磷酸腺苷(CAMP)的水平。升高的cAMP水平激活蛋白激酶A(PKA),使L型钙通道磷酸化,导致Ca+内流到心肌细胞内。这种内流从肌浆网释放细胞内的钙离子,通过钙调素调节的肌丝交叉桥的形成,进一步增加了可用于激活心肌收缩的钙离子的量。这与其他细胞内信号机制共同导致心肌收缩性增强。最后,去甲肾上腺素还能刺激其他几种心室电流,包括细胞内大量钾离子外流及钠内流,并共同导致水电解质失衡,引起各型恶性心律失常及ES的发生发展。
2.β受体反应性增强 β受体介导的儿茶酚胺效应在正常生理过程中并不占有主要地位,但是在心脏等病变的发展过程中却起着很重要的作用。跨壁复极离散已被证明是心律失常发生的一个强有力的功能性基础,β受体反应性增强在恶性心律失常的发生发展中起到重要的作用,β受体激活可增加跨室壁复极离散度,导致心肌复极异常,容易触发室性心律失常。
3.希氏-浦肯野系统传导异常 希浦系统传导异常可能参与ES,有证据表明浦肯野网络在VF的发生和持续过程中起着关键作用,异位激动不仅能诱发VF和VT,而且阻止正常窦性起搏点激动的下传,促使恶性心律失常持续性的发生与发展。
二、电风暴的治疗
(一)急性期治疗
ES患者应立即进行血流动力学不稳定评估,并应根据高级心脏生命支持(advanced cardiac lifesupport,ACLS)进行治疗,患有室性心律失常风暴,有脉搏且血流动力学不稳定的患者应接受同步心脏复律;收缩功能差或快速室性心律失常的患者可能需要多次电复律或除颤。稳定的ES患者和因血流动力学不稳定而接受复律的患者,应立即开始静脉注射抗心律失常药物和β-受体阻滞剂。推荐的方法是静脉注射胺碘酮(在10分钟内静脉注射150mg,然后静脉注射1mg/min,持续6h,然后再静脉注射0.5mg/min,持续18h)。在胺碘酮和/或利多卡因和反复心脏复律的难治性ES中,β-受体阻滞剂的应用可提高1周和1年的存活率。首选β-受体阻滞剂是普萘洛尔(前48h每6h 40mg,根据复发性室性心律失常的需要额外静脉注射剂量)。也可以对ES的患者进行早期风险分层以确保护理。高风险包括血流动力学不稳定,此外左心室射血分数低于30%,中至重度肾功能不全和严重的慢性阻塞性肺疾病。那些被确定为高危患者应转入重症监护室,在那里可以根据需要提供机械通气和循环支持,且应考虑尽早使用镇痛药和镇静药。首选药物是苯二氮卓类(如咪达唑仑)和短效止痛药(如芬太尼),它们能够在不产生负性肌力的情况下提供有效的作用效果。丙泊酚是一种短效全身麻醉剂,通过与γ-氨基丁酸受体的相互作用而起作用,但是,由于其负性肌力作用可导致心源性休克,因此应谨慎使用。另外,右美托咪定是一种高选择性α2肾上腺素受体激动剂,它除了有镇静镇痛作用,还可以使迷走神经兴奋性增加,减少儿茶酚胺释放。但是,它可能会导致低血压和心动过缓,应谨慎使用。
(二)抗心律失常药
根据Vaughan Williams分类,有四类抗心律失常药物:①一类快速钠通道阻滞剂;②二类b-阻滞剂;③三类复极钾电流阻滞剂;④和四类非二氢吡啶钙通道阻滞剂。除β受体阻滞剂外,所有抗心律失常药物在一级或二级预防室性心律失常患者心源性猝死时均不能提高生存率。然而,这些药物的使用对一些患者控制心律失常和改善症状是必不可少的。
1、β-受体阻滞剂
ES的患者,尤其是多次ICD电击的患者,交感神经张力增加,可进一步诱发复发性心律失常。β-受体阻滞剂是一种重要的治疗方法,可以降低交感神经活动增强时再发VT和VF的风险;普萘洛尔对β1和β2受体均具有拮抗作用,而美托洛尔具有β-1选择性。除其外周β受体阻滞外,普萘洛尔又因其亲脂特性,可穿透中枢神经系统,阻滞中枢和交界前受体。也许正是由于这些特性,普萘洛尔似乎比美托洛尔更有效地终止ES。且Chatzidou等,发表了一项单中心、双盲的ICD60例ES患者研究。将患者随机分为两组,均给予胺碘酮静脉滴注。普萘洛尔组每6h服用40mg,美托洛尔组前48h每6h服用50mg。结果表明,普萘洛尔组(3h)终止室性心律失常的时间明显早于美托洛尔组(18h),进一步表明普萘洛尔较美托洛尔有效。然而,对于严重收缩功能障碍的患者,尤其是需要肌力支持和失代偿性心力衰竭的低血压患者,应密切监测β-受体阻滞剂的应用。
2.胺碘酮
胺碘酮为Ⅲ类抗心律失常药物,它抑制内向去极化Na+和L-型Ca²+(ICaL)电流和几种外向去极化K+电流,并发挥非竞争性a-和β-肾上腺素拮抗作用,即它表现出I、Ⅱ、皿和IV类抗心律失常作用。胺碘酮被广泛用于治疗反复发作的室性心律失常,作为一种独立药物,静脉使用胺碘酮(1g/d)可在24h内有效地终止VT和VF周期。它即使在其他药物(如美西律、利多卡因或普鲁卡因胺)无效的情况下,仍能在静脉注射后24h内抑制40%的患者的室颤。但胺碘酮的长期使用往往受到其相关毒性的限制,包括肝功能不全、甲状腺功能减退和甲亢、肺纤维化以及最显著的促心律失常作用。且它被推荐用于结构性心脏病患者,在这些患者中,IC类抗心律失常药物是相对禁忌的。出于安全考虑,慢性胺碘酮治疗应作为更明确的治疗选择(如导管消融)的桥梁,必须定期评估药物毒性。且有研究表明静脉注射胺碘酮和口服普萘洛尔联合治疗ICD患者ES安全有效,比静脉注射胺碘酮和美托洛尔联合治疗有显著益处。
3.索他洛尔
索他洛尔一种外消旋体混合物,包括D-异构体及L-异构体。D-异构体作为Ⅲ类钾通道阻滞剂,L-异构体作为非选择性b-阻滞剂。它通过与β受体结合,从而抑制交感神经兴奋,减少细胞离子通道的儿茶酚胺增高,刺激心肌收缩,延长动作电位与心房旁路的有效不应期,从而起到抗心律不齐的作用。在心肺除颤器患者的最佳药理学治疗(optical)试验中,它在减少ICD电击方面是有效的,但并不优于单独或联合β受体阻滞剂和胺碘酮。当持续的室性心动过速对β受体阻滞剂无反应,可考虑索他洛尔。
4.植入式心脏复律除颤器(ICD)
植入ICD可以降低患有结构性心脏病和难治性室性心律失常的患者的死亡率。电风暴急性期禁止植入ICD。植入ICD作为结构性心脏病患者的继发性预防,无论结构性心脏病患者是否发生持续性室性心动过速,无论其血流动力学是否稳定,只要排除了可纠正的可逆原因,例如急性心肌梗死,心律失常药物作用或电解质紊乱,均应予以植入。
5.导管消融(catheterablation,CA) CA可有效控制ES复发,即利用导管电极在心脏中标测和消融来治疗ES。由于大多数ES是以基本折返机制为特征的单形性室性心动过速发作,多为急性心肌梗塞或非缺血性心肌病(NICM)进展后,心脏结构发生变化,由于纤维化导致疤痕形成。30%~50%的NICM患者可检测到心外膜斑状纤维化和传导异常。因此CA是阻止ES发作的重要解决方案。随着经验的增加和消融技术的快速发展,室性心动过速导管消融可以安全且并发症发生率低。总之,CA在ES管理中具有重要作用,它在减少心律失常和ICD电击方面优于药物治疗。
6.星状神经节阻滞(stellate ganglion blockade,SGB)
交感神经系统在引发和驱动电风暴中起着不可或缺的作用,交感神经系统包括多种非肾上腺素能途径和神经调节剂,它们不受这些药物的影响。对于患有药物难治性电风暴的患者,SGB可以在72h内消除或显著减轻难治性室性心律失常发作和ICD电击的负担。但在许多危重病和血流动力学不稳定的患者中,CA及紧急手术切除左心交感神经对ES患者来说是困难的,所以超声引导下经皮星状神经节阻滞(percutaneous stellateganglion blockade,PC-SGB)(一种床边程序)是治疗ES的一种替代且可能有效的治疗方法,它是目前侵入性最小的方法,且有助于改善患者的选择,以进行更明确的心脏去神经手术。即PC-SGB可以作为安全有效的临时措施,然后才能确定性治疗。SGB的即时和有效性可能挽救生命。
7.心脏交感神经去神经支配术(cardiac sympathetic denervation,CSD)
通过CSD可以实现永久性的神经轴阻滞,影响心脏的传入和传出神经支配。CSD切除的是左或双侧星状神经节的下半部和T2-T4胸神经节。CSD是治疗对抗心律失常药物和CA无效的结构性心脏病患者室性心律失常的有效方法。此外,引起ICD电击的多型VT和VF发作可能不适合CA,可考虑CSD治疗。交感神经系统在室性心律失常风暴的发生、维持和终止中起着至关重要的作用,所以CSD降低交感神经活性可显著减轻难治性室性心律失常负担。CSD已被证实能提高室颤的阀值,对于难治性室性心律失常合并结构性心脏病和先天性LQTS的患者,应考虑胸腔镜左心交感神经去神经术(video-assisted thoracoscopic-left cardiac sympatheticdenervation,VAT-LCSD)。且有病例证明左胸交感神经切除术是治疗冠状动脉搭桥术后难治性电风暴的有效方法。
8.其他治疗 针对难治性的ES,提出了许多替代方法。序贯、同时和双极消融术是射频消融术的变体,其目的是扩大病灶的大小,以靶向深部壁内室性心动过速。半生理盐水,代替常规的生理盐水作为射频消融术的冲洗剂,也可用于对壁内基质造成更大的病变。针消融是一种新的技术,将一个小27测量电极插入到心肌1cm,用于壁内消融。手术冷冻消融在治疗难以治愈的非缺血性心肌病室性心动过速的病例中被证明是有效的。经冠状动脉乙醇消融也有报道作为结构性心脏病的难治性室性心动过速的替代治疗。经静脉乙醇消融术在壁内室性心律过速中可能有用,特别是在左室顶部,但最好由经验丰富的专家进行。
(三)特殊类型心律失常治疗
现研究表明儿茶酚胺能多态性室性心动过速(catecholaminergic polymorphic ventricular tachycardia,CPVT)是由编码心肌细胞肌浆网上兰尼丁受体(RyR2)或肌浆网蛋白集钙蛋白2(CASQ2)基因突变引起的。RyR2突变是CPVT常染色体显性型的原因,而CASQ2突变罕见,是隐性型的原因。这些突变引起心肌细胞钙平衡紊乱,通过触发活动导致多型室性心动过速。现普遍使用β受体阻滞剂,已经提高了生存率。ICD被证明可将CPVT患者从心搏骤停中解救出来,但是反复的ICD电击会导致永久性心律失常。ICD放电可能导致儿茶酚胺的过度释放,这在儿茶酚胺激活的情况下尤其有害。氟卡胺和神经节切除术是治疗难治性病例的新兴治疗策略。氟卡胺的机制可能与直接抑制RyR2有关,尽管这已经被质疑。理论上当与β-受体阻滞剂联用时,总体是有益的。临床上,氟卡胺单一疗法可能仍然对那些真正不愿意或不能服用β受体阻滞剂的患者有保护作用。目前的指南指出,氟卡胺可作为β受体阻滞剂治疗室性心动过速或晕厥患者的辅助治疗。
ES是威胁生命的紧急医疗事件,且预后不良,其管理措施上需要多种方法。包括:识别和纠正其诱发因素及病因、ICD的管理、药物和非药物性的治疗。虽然有多种治疗措施,但是其病情发展迅速,临床上仍有较高的死亡率,目前关于SGB及CSD等治疗方式也越来越得到重视,且ES是个综合管理的过程,早期识别、及时处理、有效管理均是重要组成部分。随着对ES的不断认识,也需要更多的研究为ES治疗工作提供新的措施和方法。
-END-
声明:本文转载自<心脏病学文献分享>,以上仅代表作者本人观点,仅用于学习交流,版权归原作者所有。













