
近年来,虽然癌症早筛、诊断和治疗等方面都取得了较大的进展,但是绝大多数癌症晚期转移性患者的临床获益仍十分有限,除了极少数例外,大多数患者都无法治愈。已有研究表明,绝大多数与癌症相关的死亡(约90%)是由转移性肿瘤而非原发性肿瘤引起[1]。
癌症转移是一个复杂过程,肿瘤细胞通过基底膜侵入并渗入周围的脉管系统,并在继发性部位定植。为了成功转移,肿瘤细胞必须动态适应不断变化的微环境。线粒体是生物能供应、生物合成和信号传导的细胞器,是压力感应不可或缺的一部分。线粒体可帮助细胞快速适应微环境,是肿瘤发展中重要的细胞器。
近日,来自德国癌症研究中心和西班牙巴塞罗那科学技术学院的研究团队在国际顶级期刊Nature上发表题为“Mitochondrial RNA modifications shape metabolic plasticity in metastasis”的研究文章。研究发现,线粒体RNA中胞嘧啶5碳甲基化(m5C)对线粒体蛋白合成速率有重要的调节作用,可影响线粒体的代谢过程,进而影响癌症细胞的转移和侵袭。

文章发表在Nature上
线粒体是细胞中重要的能源工厂,并负责合成氧化磷酸化(OXPHOS)过程中13个蛋白亚基。线粒体中用于转运甲硫氨酸的tRNA,通常带有m5C(胞嘧啶5碳位置甲基化)和f5C(胞嘧啶5碳位置甲酰基化)修饰。该研究证明了线粒体RNA的m5C和f5C两种修饰缺失可以影响蛋白翻译速率,从而使线粒体的能量代谢从氧化磷酸化转向糖酵解。进一步分析发现,肿瘤中线粒体RNA的m5C和f5C缺失可以减少癌细胞的转移和侵袭。以上结果意味着,癌症患者进行临床治疗时,可以有一个额外选择,即通过抑制线粒体中m5C和f5C修饰来抑制癌细胞的转移和扩散,从而提高临床获益。
研究人员通过化学辅助亚硫酸氢盐测序(fCAB-seq),在线粒体基因组中探索甲基化位点(图1a)。和预期一致,m5C和f5C修饰发生在tRNAMet的34碱基位置(图1b)。通过在癌细胞中采用RNA干扰方法抑制甲基转移酶NSUN3(图1e-1n)确认了NSUN3在tRNA修饰中的作用(图1e和1d)。
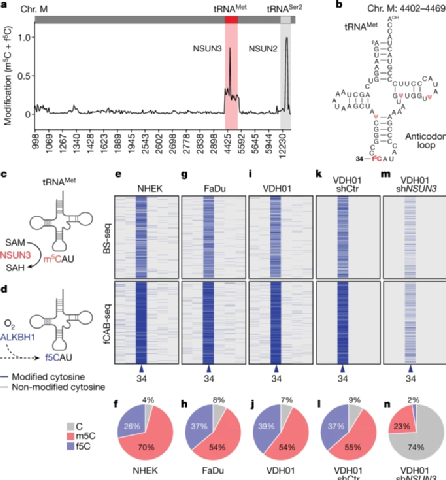
图1. 线粒体 tRNA中m5C和f5C的检测。来源:Nature
研究人员通过将O-炔丙基嘌呤霉素(OP-puro)掺入到新生肽链中,并检测量化这一过程,以判断翻译的速率。结果显示,NSUN3被抑制时,新生蛋白质的合成显著减少(图2a和2b)。通过质谱法对三羧酸循环(TCA)的代谢物进行检测,发现随着m5C和f5C修饰的减少(sh#1表示甲基转移酶NSUN3被抑制,MUT表示NSUN3失活),TCA代谢物也随之减少(图2c)。同时,在m5C和f5C修饰缺陷型癌细胞中,基础细胞外酸化率(ECAR)总体较高(图2f)。进一步检测ATP的生产来源,发现在多种癌细胞中m5C和f5C修饰被抑制后,ATP的生产来源从依靠氧化磷酸化转向糖酵解。与此同时,研究人员检测到NSUN3缺陷细胞中线粒体的形态看起来更偏圆形,每个线粒体的嵴数量减少(图2h-k)。总而言之,mt-tRNAMet中的RNA修饰m5C和f5C充当细胞能量需求的传感器并相应地调整线粒体功能(图2l)。
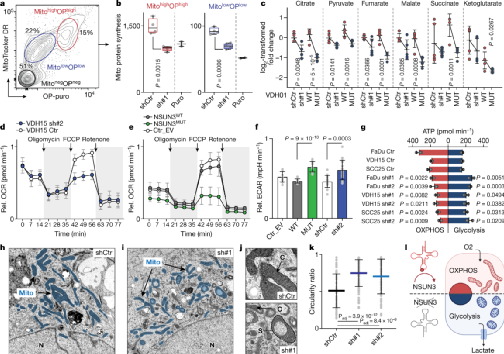
图2. 线粒体m5C调控肿瘤细胞的能量代谢。来源:Nature
已知线粒体与肿瘤发生的大部分方面有关,为了研究线粒体m5C对肿瘤发生产生了哪些影响,研究人员使用小鼠进行了肿瘤原位移植试验。设置了过表达野生型(WT)NSUN3蛋白和NSUN3酶失活(MUT)以及sh#1 NSUN3蛋白抑制组,用以验证肿瘤发生过程中甲基化依赖性细胞功能。
结果显示,小鼠所有的原位移植都形成了肿瘤,大多数肿瘤(75%)形成了转移,在MUT组中,淋巴结和肺的癌细胞转移持续减少(图3a和3b)。为了排除原位肿瘤大小影响转移率的可能性,研究人员将继发性肿瘤的尺寸和原发性肿瘤的尺寸进行匹配的均一化,结果显示当NSUN3被失活或者抑制时,该比率始终较低(图3C)。以上结果证明,线粒体m5C修饰对癌细胞转移产生了影响。
和肿瘤细胞的实验结果一致,原位移植的癌组织也呈现出主要依赖糖酵解获取能量的现象。通过对肿瘤进行组织学检查,NSUN3被抑制的肿瘤表现出葡萄糖转运蛋白1(GLUT1)上调(图3d和3e)。在NSUN3失活的情况,编码氧化磷酸化途径蛋白质的RNA受抑制成都最高(3f和3g),通过基因集富集分析(GSEA)进一步证实了这一结果(图3h)。
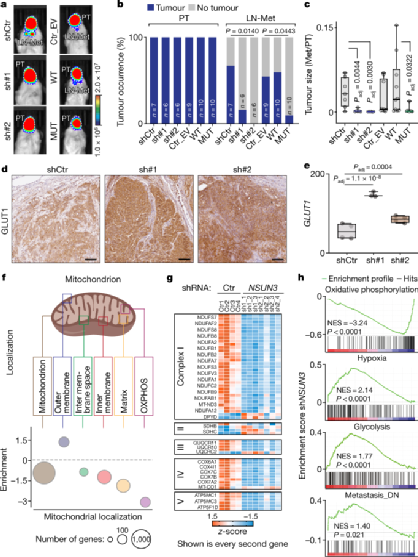
图3. 癌细胞的转移需要线粒体m5C修饰。来源:Nature
该研究表明,线粒体RNA修饰水平的动态调整可促进癌细胞转移。虽然氧化磷酸化途径严格依赖于细胞溶质和线粒体蛋白质合成机制,但研究人员发现降低线粒体RNA中m5C的水平,足以阻止从糖酵解到氧化磷酸化(OXPHOS)的代谢转换。进一步分析发现,癌细胞转移需要线粒体m5C来激活原发性肿瘤的侵袭。NSUN3作为一种负责修饰RNA的酶,是具有功能专一性的,只用于修饰m5C的形成,因此是一种非常有前景的药物靶点,是阻止癌细胞在肿瘤发展后期扩散的潜在治疗方法。
[1] Lambert, A. W., Pattabiraman, D. R., & Weinberg, R. A. Emerging biological principles of metastasis. (2017). Cell, 168(4), 670-691.
[2] Delaunay, S., Pascual, G., Feng, B. et al. Mitochondrial RNA modifications shape metabolic plasticity in metastasis. Nature (2022). https://doi.org/10.1038/s41586-022-04898-5














